オンコロジー入門(1)
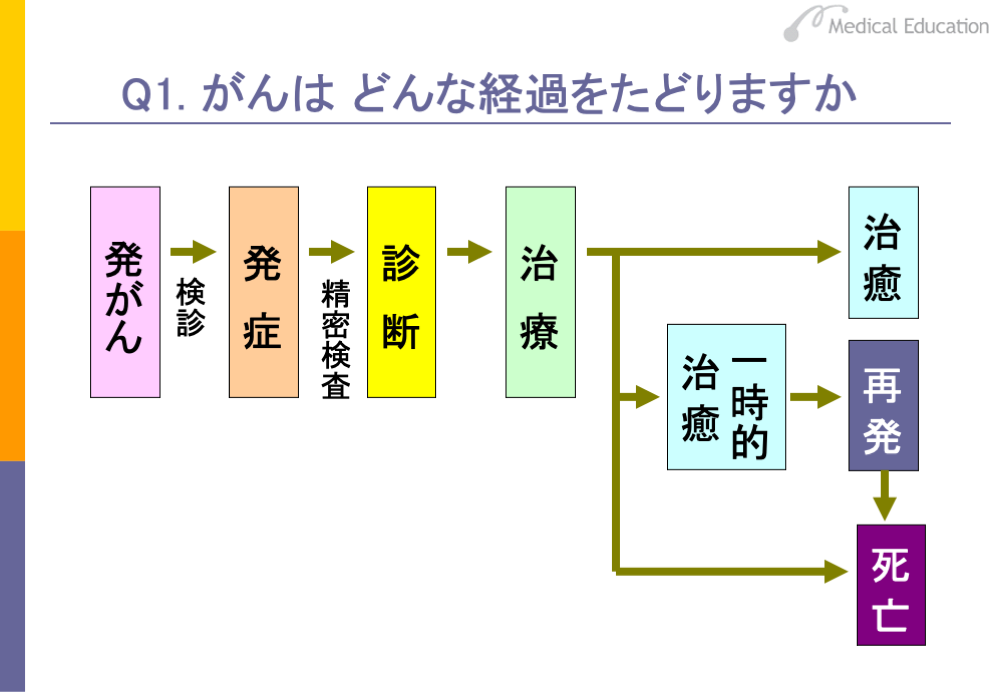
がんはどのような経過をたどるのでしょうか。通常は、がんになってもすぐには症状が出てきません。検診等で疑われ、病院で精密検査を受けた結果、がんと診断される場合もありますが、進行して症状が出てきてから、診断される場合も多々あります。
がんと診断され、治療を受けた結果、治癒する場合もあります。また、一時的に治癒はしますが、再発する場合もあります。再発した場合は、治癒するケースは少なく、大半は死に至ります。治療を受けてもよくならず、そのまま死に至るという不幸な転帰をたどる場合もあります。
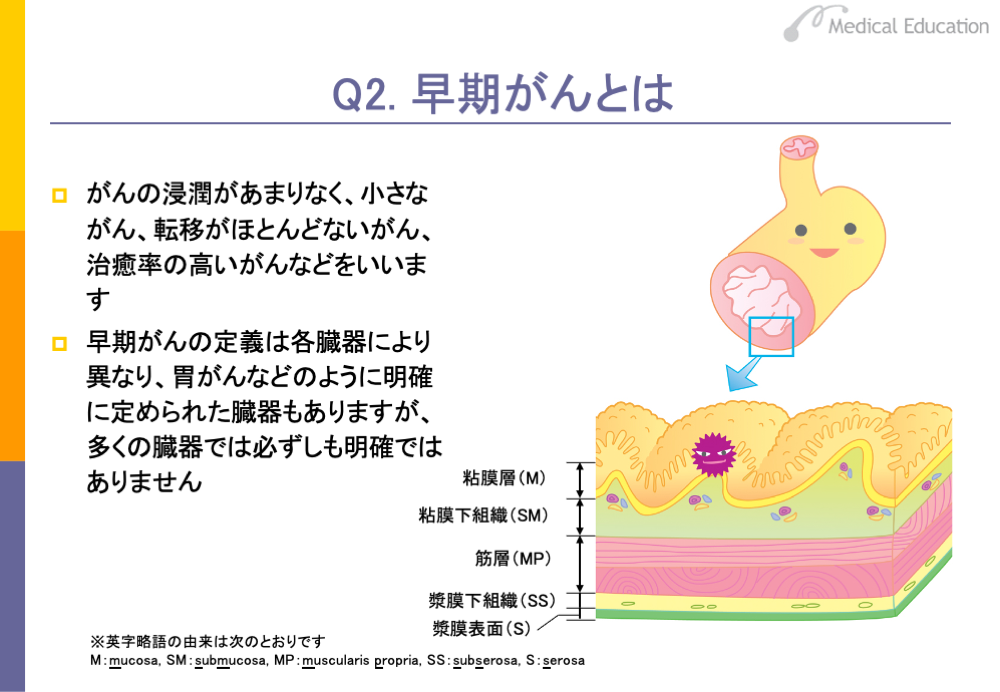
早期がんとは、進行がんに対応する言葉です。早期がんの定義は臓器によって異なります。胃がんや大腸がんなどは、粘膜層あるいは粘膜下組織にがんがとどまっているものを早期がんと明確に定義しています。しかし、他の多くの臓器では早期がんは明確に定義されていません。
一般的には、ほとんど転移がないために治療によって長期の生存が得られる可能性のある場合を、早期がんといいます。
なお、がんが上皮内にとどまり、浸潤していない状態を上皮内がんといいますが、
上皮内がんは早期がんに含まれます。上皮内がんは、carcinoma in situと呼ばれ、cisやTisと表記されます。
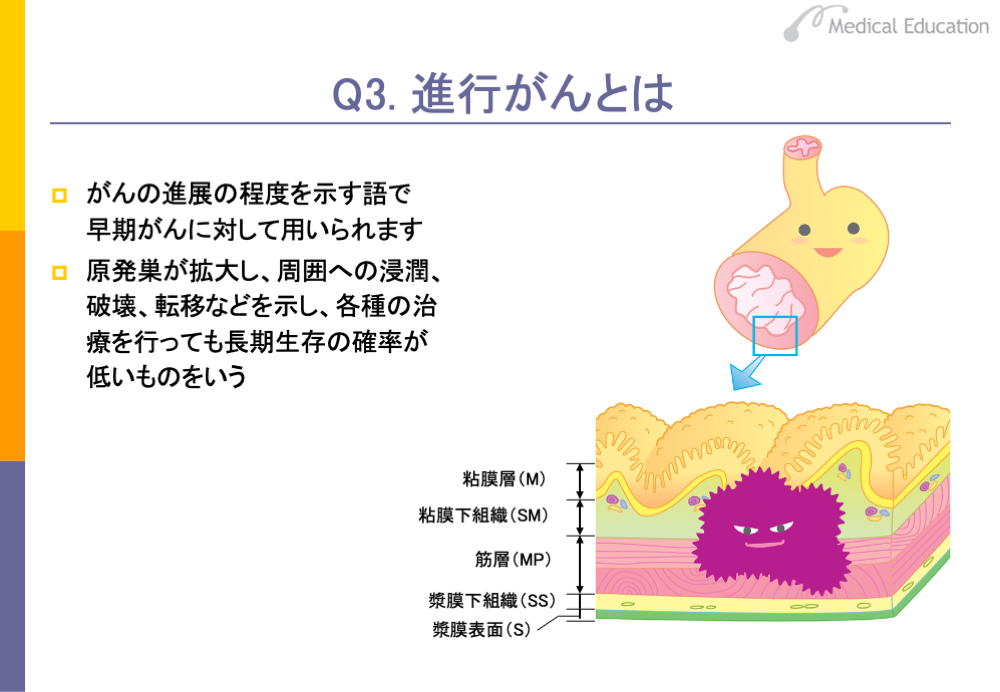
早期がんに対して、進行がんという言葉があります。進行がんは局所における浸潤、破壊が著しく、リンパ節転移などを起こす頻度が高まり、各種の治療を行っても長期生存の確率が低いものをいいます。進行がんになると、周囲の臓器への浸潤や遠隔転移が起こりやすくなります。
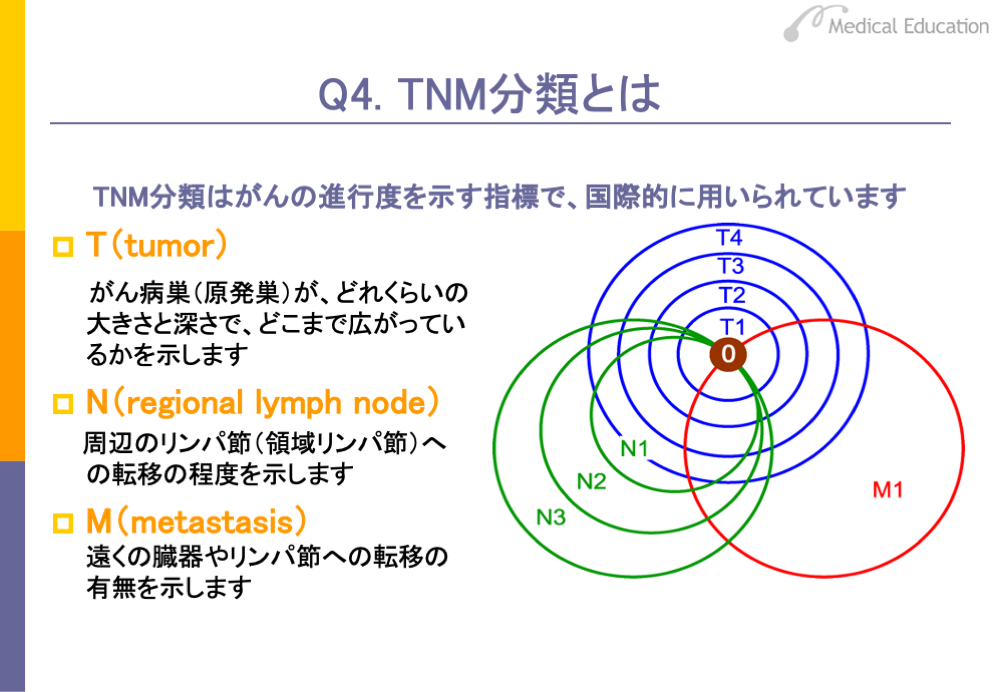
がんの進行度を示す指標としては、国際的にはUICC(国際対がん連合)のTNM分類が用いられています。 TNM分類はT因子、N因子、M因子の3つの因子による分類から成り立っています。
T(tumor)因子による分類はT分類と呼ばれ、がん病巣がどれくらいの大きさと深さで、どこまで広がっているかを示すものです。T0からT4で表します。
N(regional lymph node)因子による分類はN分類と呼ばれ、 領域リンパ節への転移の程度を示すものです。領域リンパ節とは、がんの発生した臓器に付属しているリンパ節のことで、所属リンパ節と呼ぶこともあります。転移がある領域リンパ節の個数などによって、各臓器ごとにN0からN3で表します。
M(metastasis)因子による分類はM分類と呼ばれ、遠隔転移の程度を示しています。遠くの臓器、領域リンパ節以外のリンパ節、すなわち遠隔リンパ節への転移の有無を示します。遠隔臓器への転移がないものをM0、転移があるのものをM1で表します。
TNM分類では、これら3つの分類を組み合わせて、T2N1M0のように進行度を表現します。
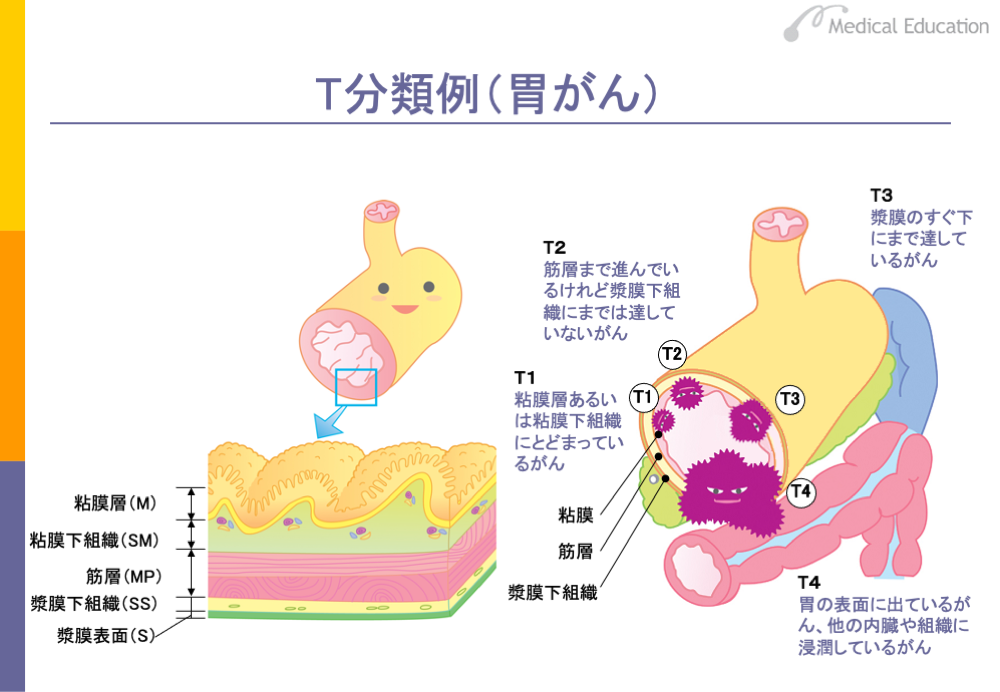
T分類は、先に示したようにがんの広がりを5段階で示していますが、臓器によって分類の方法が異なります。胃がんを例にみてみましょう。
胃がんの場合は、がんが到達した胃の壁の深さに応じて分類されています。がんの原発巣を認めない場合をT0、粘膜層あるいは粘膜下組織にがんがとどまっている場合はT1、T1を超えて筋層まで達している場合はT2、筋層を超えて漿膜下組織にまで達している場合はT3に分類されます。さらに、漿膜にまで達して胃の表面に露出していたり他の臓器に浸潤している場合はT4に分類されます。また、がんの浸潤の深さが不明なものはTXで表されます。
なお、T1は粘膜層にがんがとどまっているT1aと、粘膜下組織にがんがとどまっているT1bに亜分類されているほか、T4はがんが漿膜表面に達しているものの、他の臓器にまでは浸潤していないT4aと他の臓器に浸潤が及んでいるT4bに亜分類されています。
乳がんでは、大きさのほか胸壁または皮膚への直接進展などで決めています。原発巣を認めない場合がT0、がんの直径が2cm以下をT1、2~5cm以下をT2、5cmより大きい場合をT3、大きさを問わず、胸壁または皮膚への直接進展があればT4としています。
このように、がんの種類によって、T分類の仕方が異なっています。
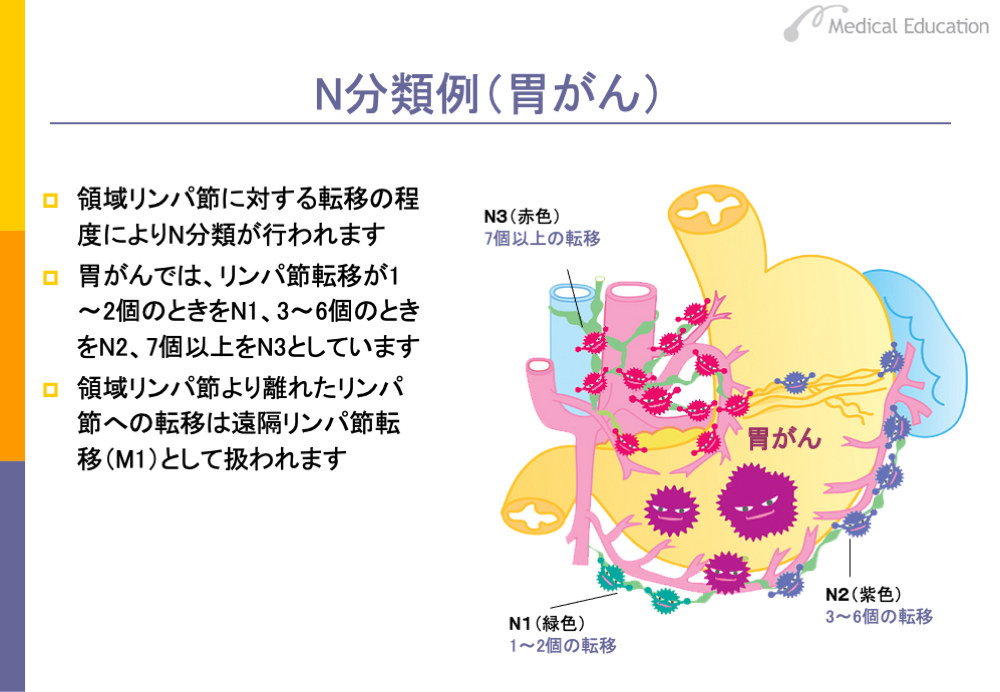
N分類は、領域リンパ節への転移の程度を表します。
胃がんを例に取ると
N1:領域リンパ節に1~2個の転移を認める
N2:領域リンパ節に3~6個の転移を認める
N3:領域リンパ節に7個以上の転移を認める
以上のように分類されています。
なお、領域リンパ節転移のないものはN0、転移の有無が不明なものはNXで表します。
また、領域リンパ節以外の離れたリンパ節への転移は遠隔転移として扱われます。
一方、乳がんでは転移リンパ節の数による分類ではなく、転移リンパ節がどの程度動くかといった触診による診断と、どの範囲のリンパ節にまで転移が及んでいるかということからN分類が行われています。
T分類と同様、N分類もがんの種類によって、分類の仕方が異なっています。
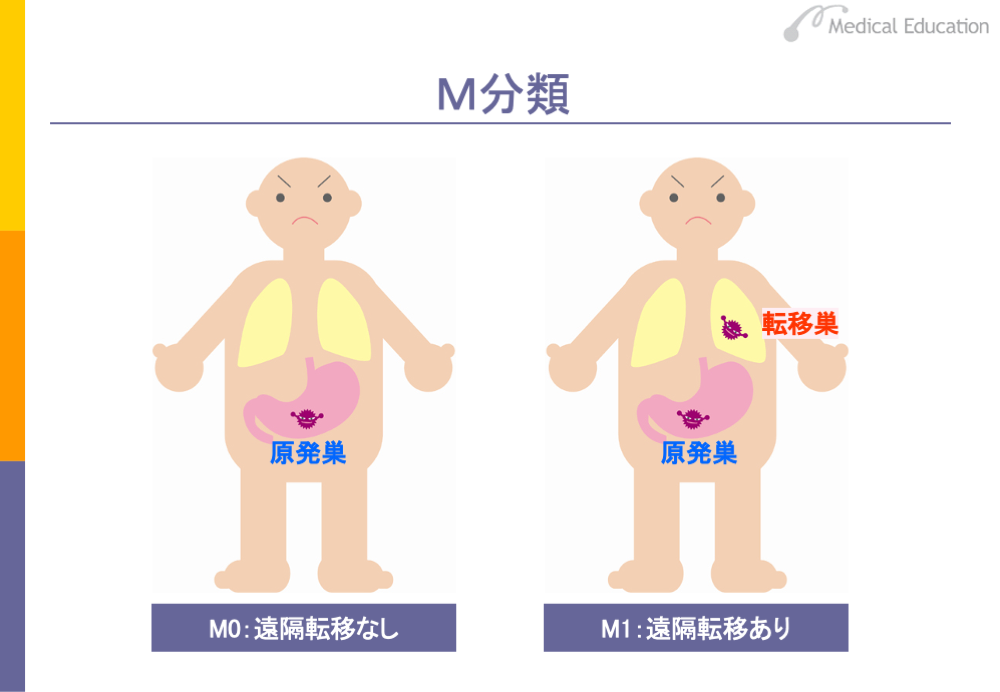
M分類は遠隔転移があるかないかで分類します。遠隔転移がある場合はM1、ない場合はM0と表します。なお、遠隔転移の有無が不明の場合はMXで表します。この分類は全臓器に共通しています。また、日本でも海外でも共通です。
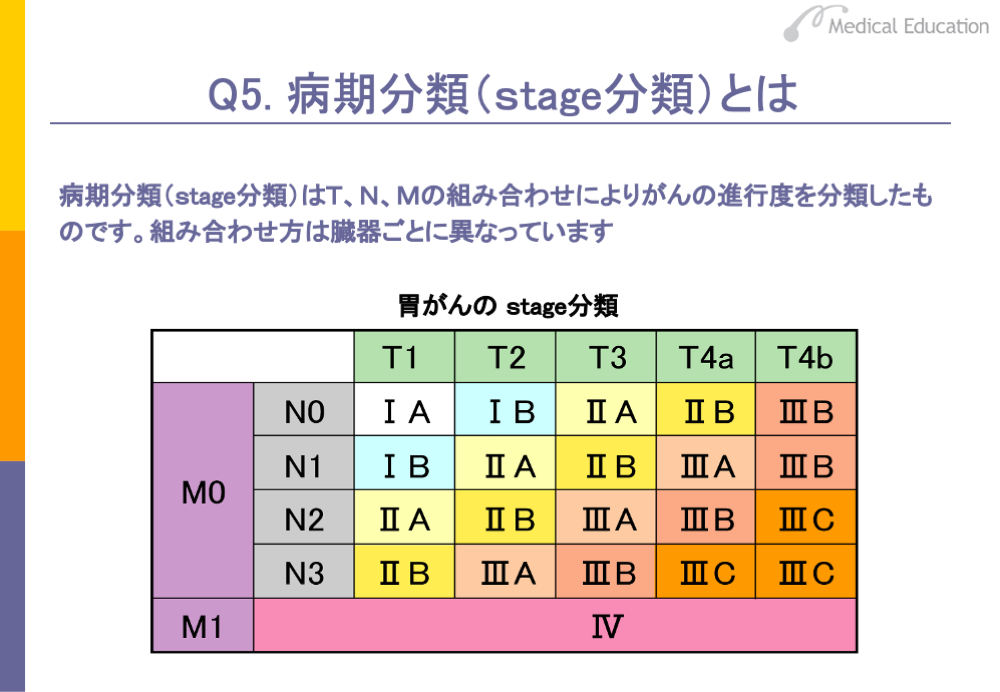
TNMによる病期分類は臓器ごとに決められており、T、N、Mの組み合わせで表すことができます。原則的にはⅠ~Ⅳの4つの期に分けられます。
スライドのように、M分類が1の場合、つまり遠隔転移がある場合はstage Ⅳということに決められています。M0の場合、つまり遠隔転移がない場合はがんの広がりを示すT分類の1~4まですべての段階と、領域リンパ節への転移の有無と程度を示すN分類である0~3の段階を組み合わせてⅠ~Ⅲ期までに分けています。
また、T1aN0M0のように、がんが上皮にとどまりリンパ節転移や遠隔転移がない場合は、stage 0と表わすことがあります。Stage 0のがんは、基本的には外科手術で100%治癒するがんということになります。
わが国ではT、N、M の組み合わせに基づいた病期分類が各「癌取扱い規約」によって取り決められています。「取扱い規約」とTNM分類でT分類やN分類などの表記や定義の仕方が異なる場合があるため、TNM分類の病期分類と日本の臨床医が用いる病期分類は少し異なっていることがあります。

「癌取扱い規約」は各臓器のがんに対する表記方法、腫瘍の状態や病理の記載法などの基本的ルールが定められています。スライドのように、臓器ごとにまとめられています。
日本では、この規約に基づき、stage分類が定められています。ただし、各取扱い規約も、最近では国際的な基準に合わせるのが基本になっており、数年に一度改訂されています。改訂ごとに、少しずつ分類の方法も変わってきています。
たとえば胃がんや大腸がんの場合、以前は1~3群という群別のN分類を定めていましたが、最近の取扱い規約の改訂では、転移したリンパ節の個数により分類するなど、TNM分類との整合性が図られています。
また、日本では臓器ごとにがんの治療ガイドラインが整備されてきています。規約にあった治療に関する事項は、ガイドラインへ移行されつつあり、棲み分けが図られています。

末期がんについては、明確な定義はほとんどされていません。
一般的に、治療上の観点から末期がんといった場合には、がんの症状が最終段階まで進行し、治療が困難な治癒の見込みのない状態と考えることができます。具体的には、がん細胞が全身に転移している状態、あるいは病期分類ではstageⅣの状態といえます。
一方、生命予後の観点からは、予後の生存期間が1ヵ月以内から3ヵ月以内、6ヵ月以内とするものまで、まちまちです。

異なる臓器にそれぞれ原発性のがんが同時に存在するものを重複がん、同一臓器内に同じ組織型のがんが多発するものを多発がんといいます。そして、多発がんと重複がんとを合わせて多重がんといいます。
なお、同一臓器内に異なる組織型のがんが存在する場合、重複がんということもあります。
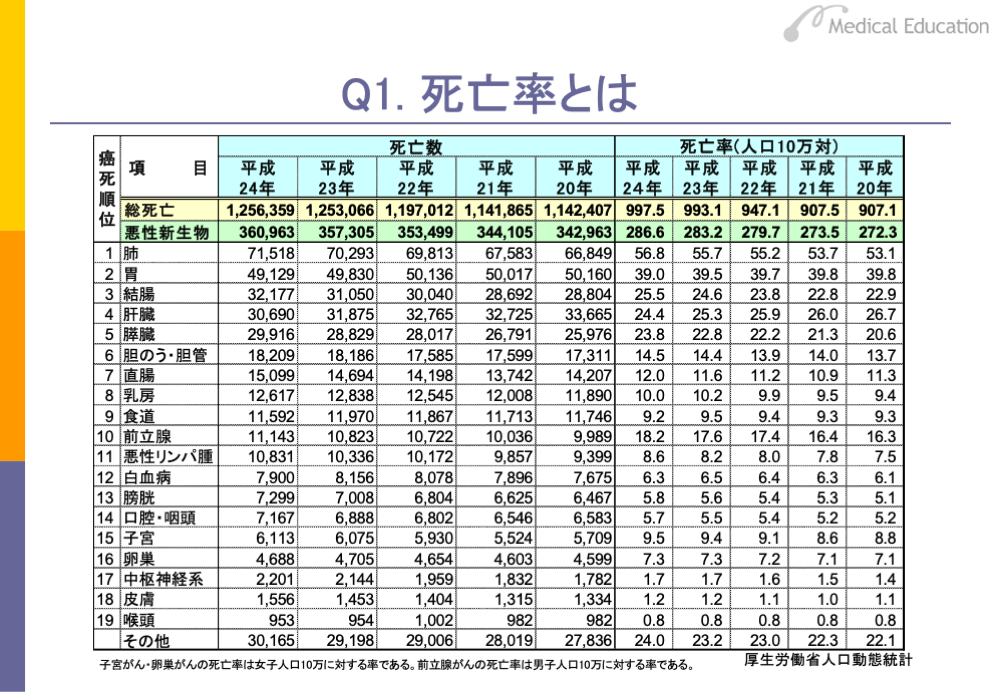
スライドは、日本における過去5年間のがんごとの死亡数と死亡率を表にしたものです。2012(平成24)年のがんによる死亡数は約36万1,000人で、ここ4年間で1万8,000人と大幅に増加しています。死亡数が最も多いのは肺がんで約7万2,000人、次いで胃がんの約4万9,000人です。第3位は結腸がんですが、直腸がんと合わせた大腸がんでは約4万7,000人が死亡しています。以下、肝臓がん約3万1,000人、膵臓がん約3万人と続いています。
ただし、海外と比較しようとする場合、人口の多い国は死亡数も多いため、そのままでは比較できません。統計的に比較しようとする場合は、表の右側のように人口10万人当たり何人ががんで死亡したかという死亡率で比較します。死亡率とは厳密には、一定期間の死亡数、たとえば1年間の死亡数を全体の人口で割った値のことをいいます。通常は小数点以下の小さな数値での表記を避けるため、人口10万人当たりの率で示しています。
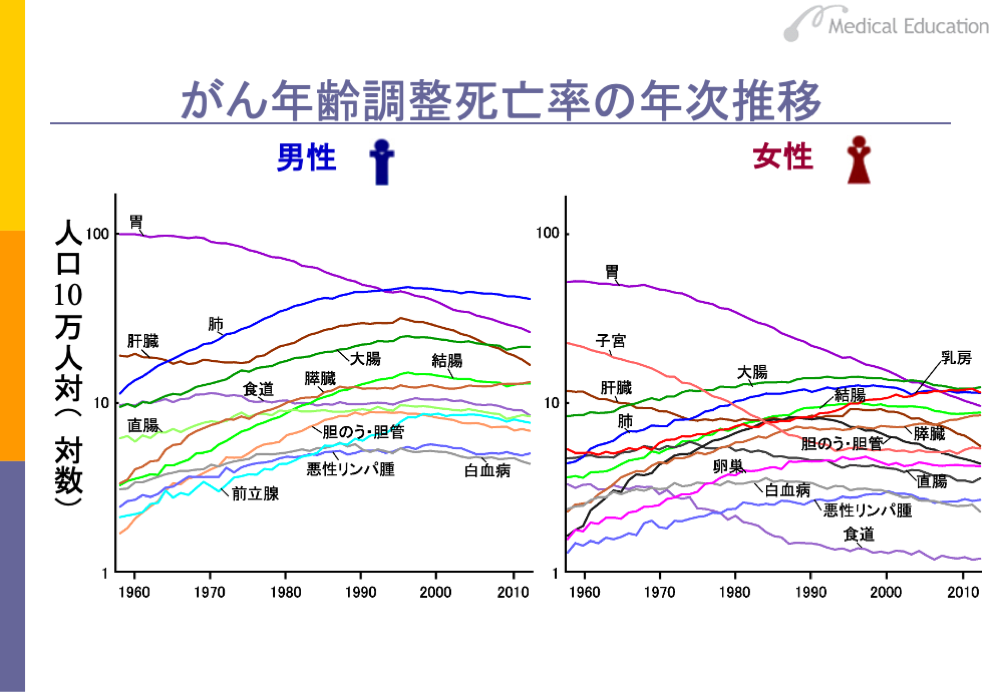
もう1つ、海外と比較する場合などに、気をつけなければならない点があります。たとえば、日本のように高齢者が多い国では、がんの発生率は高くなりますが、逆にアフリカの国々のように若い世代の多い国では低くなるなど、発生率だけでは単純に比較できない点です。このような年齢によるファクターを入れて死亡率を計算したものを「年齢調整死亡率」といいます。これにより、さまざまな国の間で、どういうがんが多く、どういうがんが少ないのかという比較ができます。
年齢調整死亡率でみると、日本の場合は男性、女性ともに胃がんの死亡率は低下しています。男性で2000年頃まで増加傾向にあった肺がん、大腸がん、前立腺がんは、2012年時点ではいずれも減少傾向にあります。女性では乳がんは増加していますが、子宮がんは低下してきています。また、膵臓がんは男女とも増加傾向にあります。

一方、実際にがんになる人が何人くらいいるのかをみた数字が、「罹患率」です。死亡数は、厚生労働省が統計をとっているため数字が明確にわかりますが、罹患数は以前の全国統計をとっていないため、明確な数字はわかりません。ただ、大阪府、熊本県など、いくつかの地域で、地域ごとの統計をとっているため、これをもとに推計することは可能です。
推計の結果、人口10万人当たりの部位別がん罹患率をみると多くの部位で男性が女性より高くなっています。死亡数で2位だった胃がんが男性では罹患率の1位になっています。2位が肺がんで、次いで前立腺がん、結腸がん、肝臓がんの順です。ただし、結腸がんと直腸がんとを合わせた大腸がんの罹患率では、前立腺がんを上回っていて3位となります。
女性の罹患率は、乳がんが最も高く、次いで胃がん、結腸がん、肺がん、子宮がんの順となっています。ただし、女性の場合も、結腸がんと直腸がんとを合わせた大腸がんでは、胃がんを抜いて2位になります。
肺がんはタバコと関連があり、女性では喫煙する人が少ないため肺がん罹患率が男性より低くなっています。
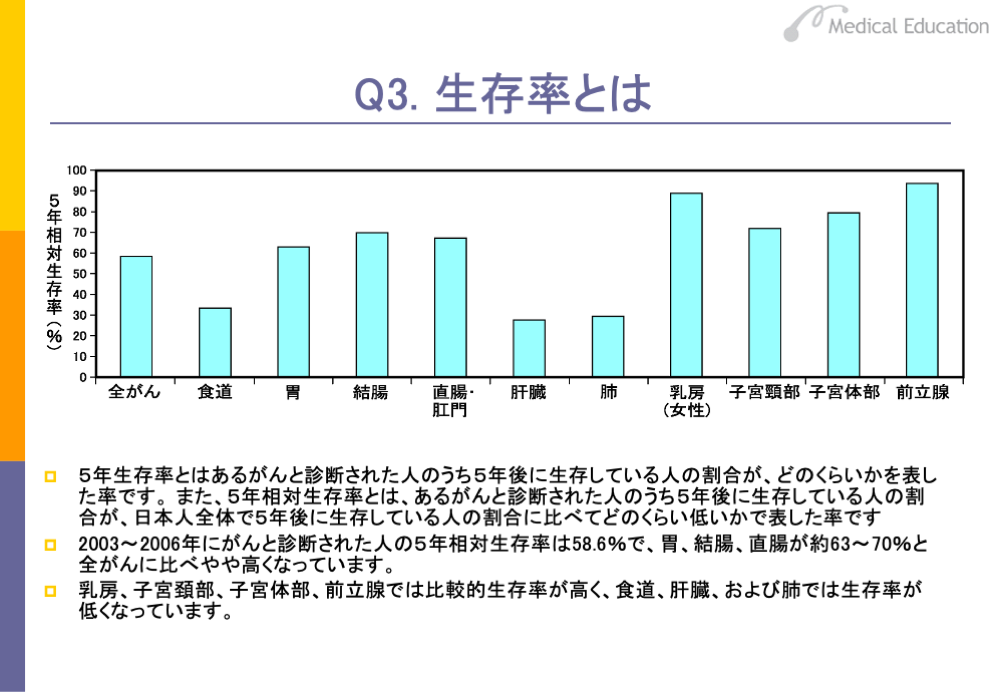
生存率でよく使われるのは、5年生存率です。5年生存率とは、あるがんと診断された人が治療を受け、その治療を受けた人のうちの何%が5年後に生きているかをみた数字です。ただし、5年相対生存率といった場合は、意味が違ってきます。5年相対生存率とは、あるがんと診断された人が、治療を受けた人全体ではなく、日本人全体の中で5年後に生きている人と比較した割合です。5年生存率と5年相対生存率は、まったく違う概念であることを理解しておきましょう。
いずれにしても、予後の悪い、つまり治療しても成績があがらないがんの場合は生存率も悪くなります。胃がんや結腸・直腸がんは罹患率は高いものの、予後はさほど悪くありません。罹患率が高く、生存率が低いのは、肝臓がん、肺がんなどです。
また、スライドには載っていませんが、喉頭および膀胱は比較的生存率が高く、甲状腺は90%以上の高い生存率を示す一方、胆のう・胆管がん、膵臓がん、多発性骨髄腫、白血病は予後が非常に悪いがんで、なかでも膵臓がんは生存率10%以下と極端に予後の悪いがんです。
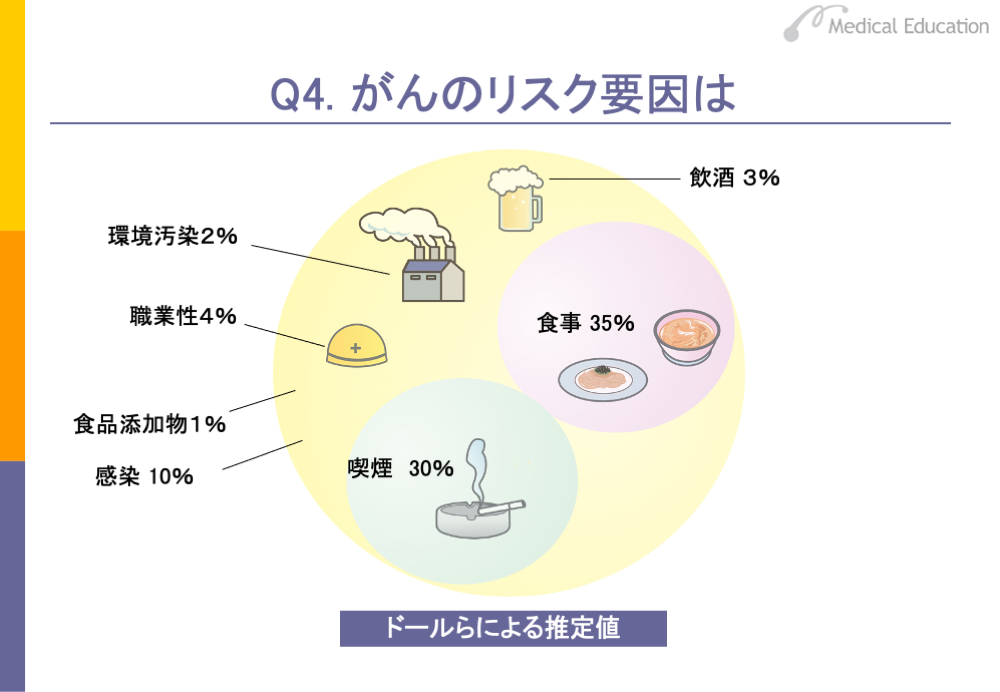
がんのリスク要因には、さまざまなものがあります。ドールらは、多くの科学論文からアメリカ人のがん死亡の原因として、どの要因がどれくらいの割合を占めているかを推定し、1981年に発表しています。
それによると、食事の割合が35%と一番高く、次いで喫煙が30%、ウイルス・細菌などの感染が10%、飲酒が3%などとなっています。個人の生活習慣に関連する要因で約7割を占めており、これらは生活習慣を改善することにより避けられると考えられます。また、感染症、職業性、環境汚染等も、努力次第で改善することは可能です。

スライドは、がんのリスク因子と、その防御因子について表にまとめたものです。リスク因子として部位を問わず多いのは喫煙です。また、最近では、高脂肪摂取ががんのリスク因子として増えています。したがって、禁煙および脂肪の摂取を控えることで、かなりのリスクを避けることができます。
がんの防御因子としては、多くのがんで緑黄色野菜があげられています。また、運動も防御因子となります。つまり、たばこを吸い、食生活では高脂肪食に偏り、野菜の摂取をおろそかにし、なおかつ運動不足という生活を送っていると、がんになる確率が高くなるということです。
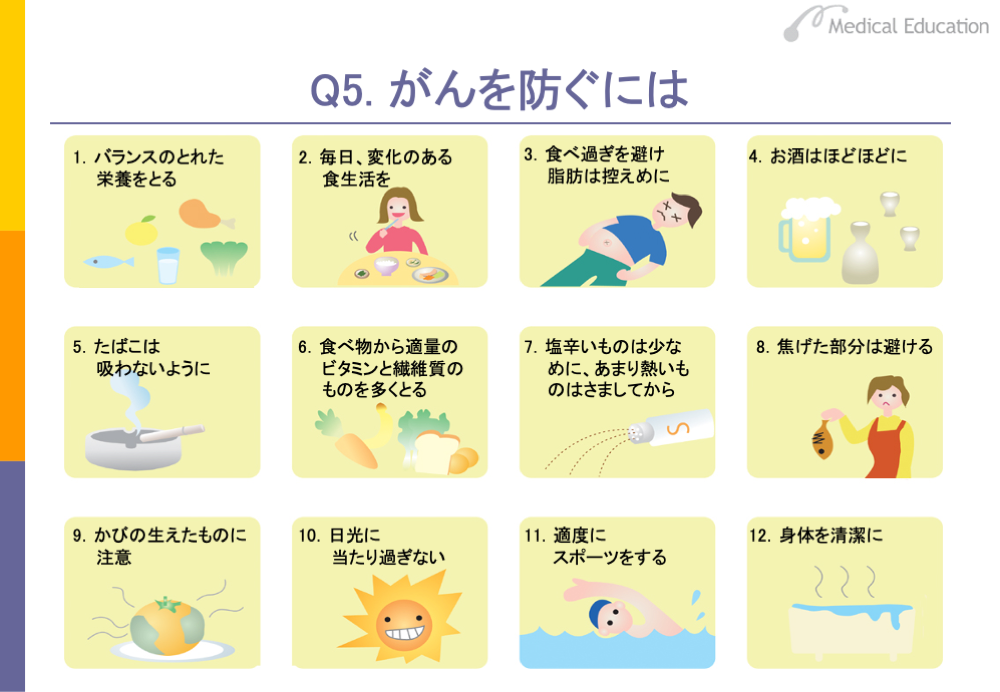
国立がん研究センターでは、がんを防ぐための注意すべき12か条を発表しています。スライドでみるように、まず、偏った食生活をやめてバランスのとれた栄養を摂ること、食べ過ぎず、脂肪をあまり摂らないように気をつけることです。また、お酒をほどほどにし、たばこをやめることも大切です。
塩辛いものは、食塩ががんのプロモーターになるため控えます。焦げた部分には、発がん物質であるニトロソアミンが含まれているため、避ける必要があります。また、かびの生えたものは、かびの中の毒素が発がん物質となります。日光も、紫外線が皮膚に当たると皮膚がんのもととなるので、当たり過ぎないなどの注意が必要です。その他、適度にスポーツをすること、身体を清潔にすることなどががんを防ぐためには必要であるとされています。
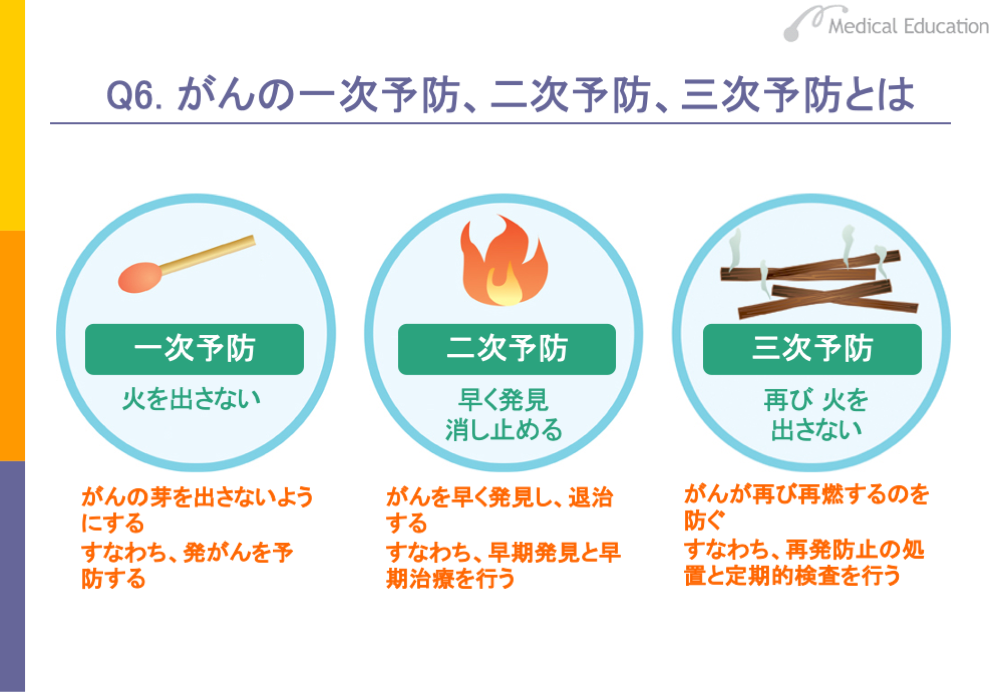
がんに対しては、一次予防、二次予防、三次予防という考え方があります。一次予防とは、火事にたとえると、火事を出さないということです。がんにならないように、栄養に気をつける、適度な運動をするなど、発がんを予防するのが一次予防です。二次予防は、火事を早くみつけ、早く消してしまう、すなわち、がんが小さいうちに早期発見、早期治療を行うことです。早期発見、早期治療により、治療成績もよくなります。
がんが上皮内にとどまっている段階で手術をすれば、ほとんどのがんは100%治るというのが現在の常識になっています。がんは決して怖い病気ではないということです。ただし、肝臓がんや胆のう・胆管がん、膵臓がん、肺がんなどは早期発見がしにくいため、生存率が悪くなっています。このうち、肺がんは診断機器が向上してきたため、早期発見が可能になり、予後が改善される可能性があります。問題は、それ以外の肝臓がんなどで、これらの早期発見が、現在のがん治療の課題の1つになっています。
三次予防は、火事になっても消火を確実に行い、再燃を防ぐことです。がんを治療した後のフォローアップをきちんと行い、がんの再発を防ぎます。再発した場合でも、定期検査等により、再発を早くみつけて早く治療することで治療成績をあげるというのが三次予防の考え方です。
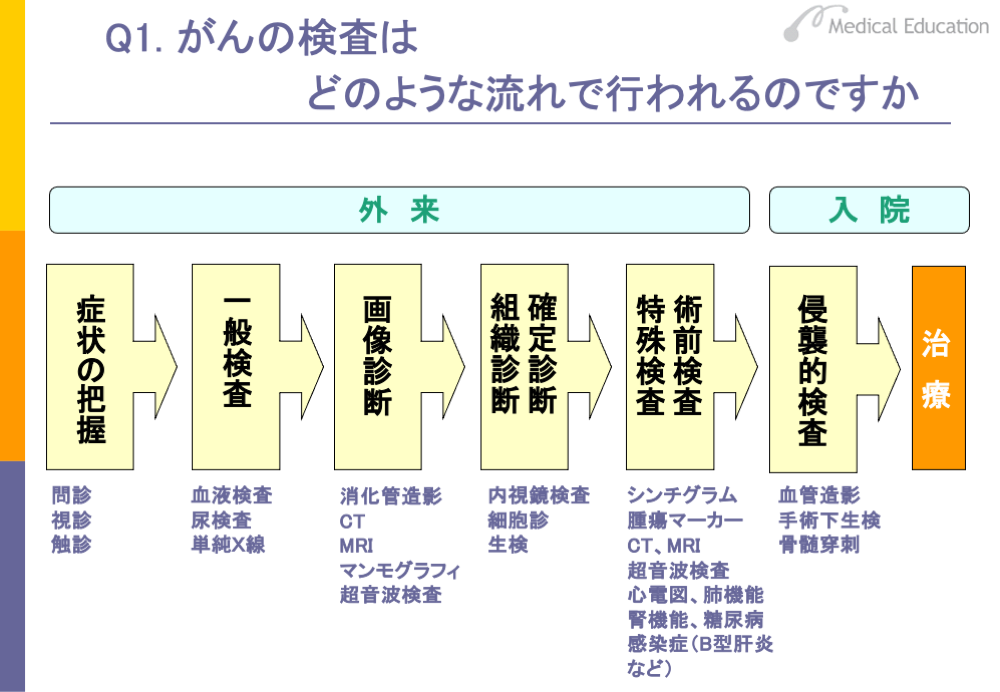
がんの検査の流れは、スライドのように外来と入院の2つに大きく分けられます。一般的には、最初に外来で問診、視診、触診等を行い症状を把握します。がんが疑われる場合は、一般検査に回します。一般検査を行った後、比較的実施しやすいCTや超音波検査などを行い、画像診断をします。消化管の場合は二重造影、乳がんの場合はマンモグラフィなどです。画像診断で、やはりがんが疑われるという場合は、組織診断を行います。疑いの強い部分の組織をとって病理で確認し、がん細胞がみつかった場合はがんの確定診断が下されます。その後、特殊検査、術前検査を経て、手術を行います。術前検査では、腎機能や糖尿病、感染症の有無等も確認します。
入院して行わなければならない検査には、侵襲的検査があります。侵襲的検査には、手術下生検、血管造影、骨髄穿刺などがあります。
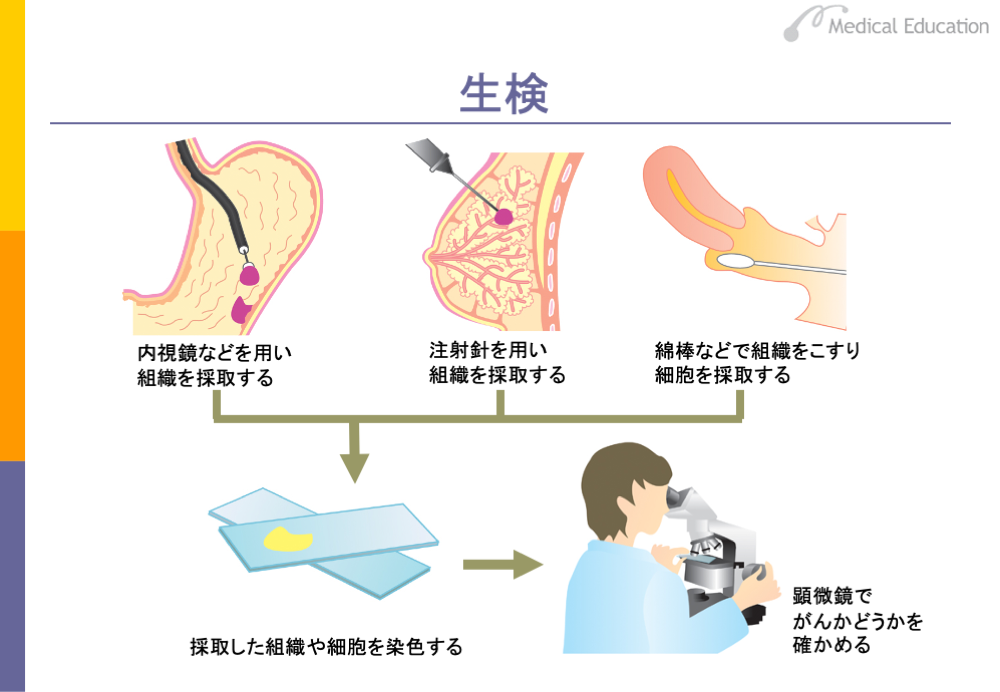
がんであるかどうかという最終的な判断は、病理診断により行います。すなわち疑わしい組織をとってきて標本を作り、病理の医師ががんかどうかを確認します。組織をとる方法としては、目でみえる場合は直接メスで組織を切り取りますが、消化管や気管支の場合は内視鏡を用いて組織を採取します。乳がんなどでは注射針を用いて組織を採取することもあります(これはニードルバイオプシーと呼ばれます)。子宮頸がんの場合は綿棒などで子宮頸部の組織をこすり、剥げ落ちた細胞を採取します。このようにして採取された組織は薄くスライスして染色し、顕微鏡でがん細胞があるかどうかを調べます。
さらに、手術をして切り取った組織も同様に標本を作り、病理の医師が検査して組織型や分化度、悪性度といったがんの性格を割り出します。
なお、「乳癌診療ガイドライン2008年版」から、センチネルリンパ節生検が標準治療とされています。
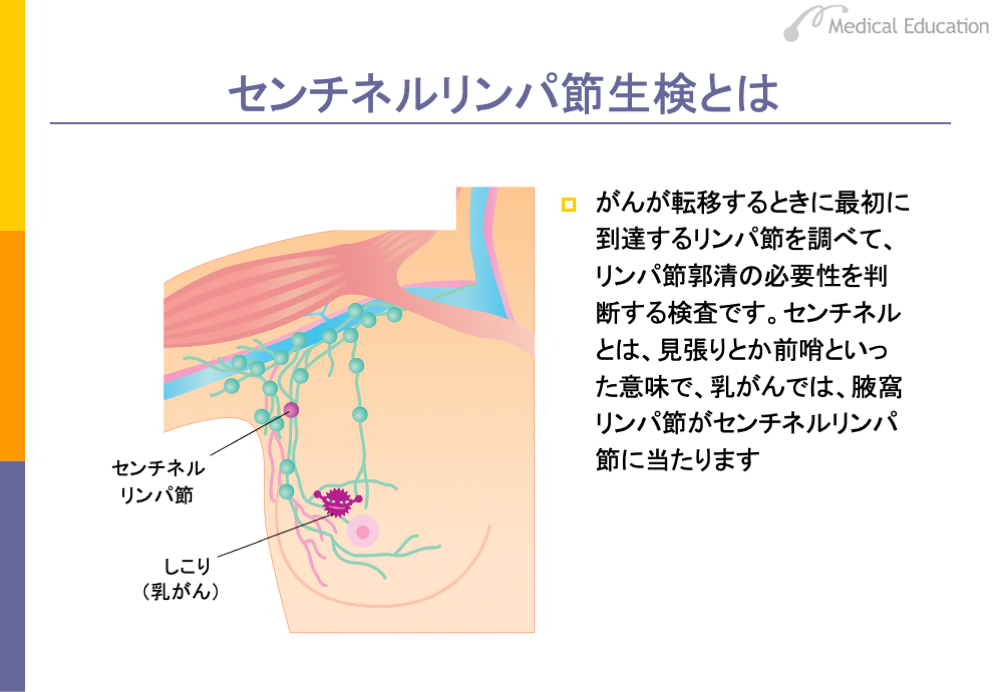
がんが転移するときに最初に到達するリンパ節を調べて、リンパ節郭清の必要性を判断する検査です。センチネルとは、見張りとか前哨といった意味で、乳がんでは、腋窩リンパ節がセンチネルリンパ節に当たります。
従来、乳がんでは、定型的乳房切除術や乳房温存術のいずれにおいても、腋窩リンパ節切除が行われてきました。そのため、リンパの流れが悪くなり、腕がパンパンにむくむなどのリンパ浮腫が起こり、患者さんの苦痛のもとになっていました。センチネルリンパ節に転移が認められなければ、その先にある他のリンパ節にも転移がないと考えられることから、腋窩リンパ節切除を省略でき、患者さんのQOLを向上することができます。
具体的には、外来または手術の前に乳がんの近くにラジオアイソトープあるいは色素を注入し、それを目印にして、センチネルリンパ節を探し出して摘出し、このリンパ節にがんが転移しているかいないかを調べ、腋窩リンパ節切除の有無を決定します。
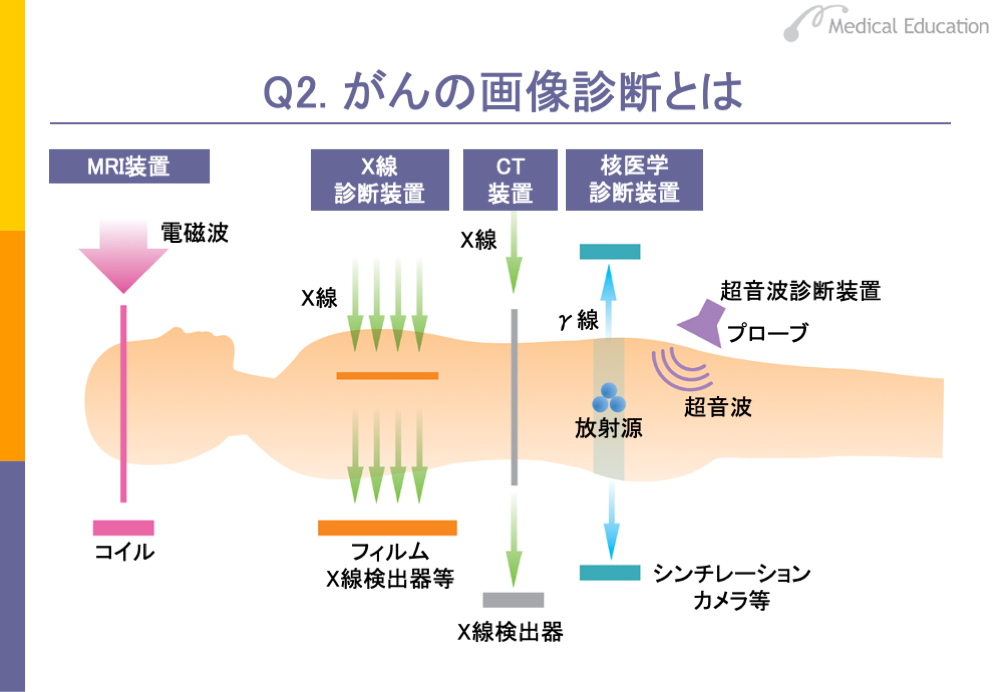
画像診断には、X線を用いたX線検査やCT検査、電磁波を用いたMRI検査などがあります。これらは病院でよく行われる検査です。超音波を用いる超音波検査も一般的です。特殊なものとしては、核医学診断装置があります。これはがん組織などに集積する性質のある放射性物質を用いて、シンチレーションカメラという特殊なカメラで体内の状態を調べる検査です。
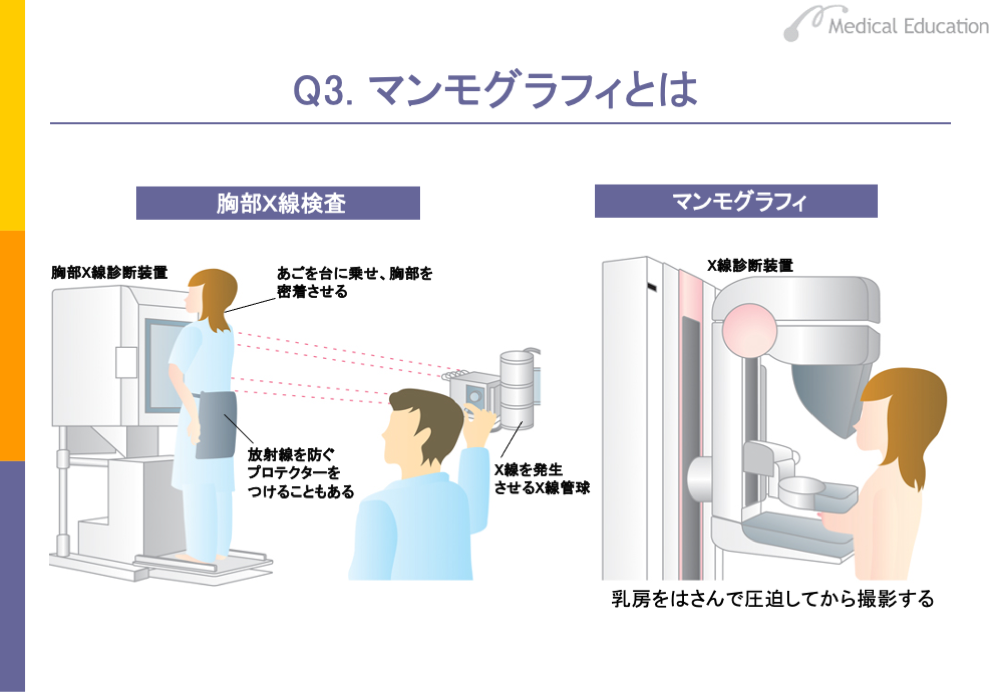
X線検査は、肺がんの検査等で行われますが、 特殊なものにマンモグラフィがあります。マンモグラフィは、乳がんの検査のみで用いられます。
スライドのように乳房を圧迫して上から放射線を当てて、がんの存在の有無を調べます。
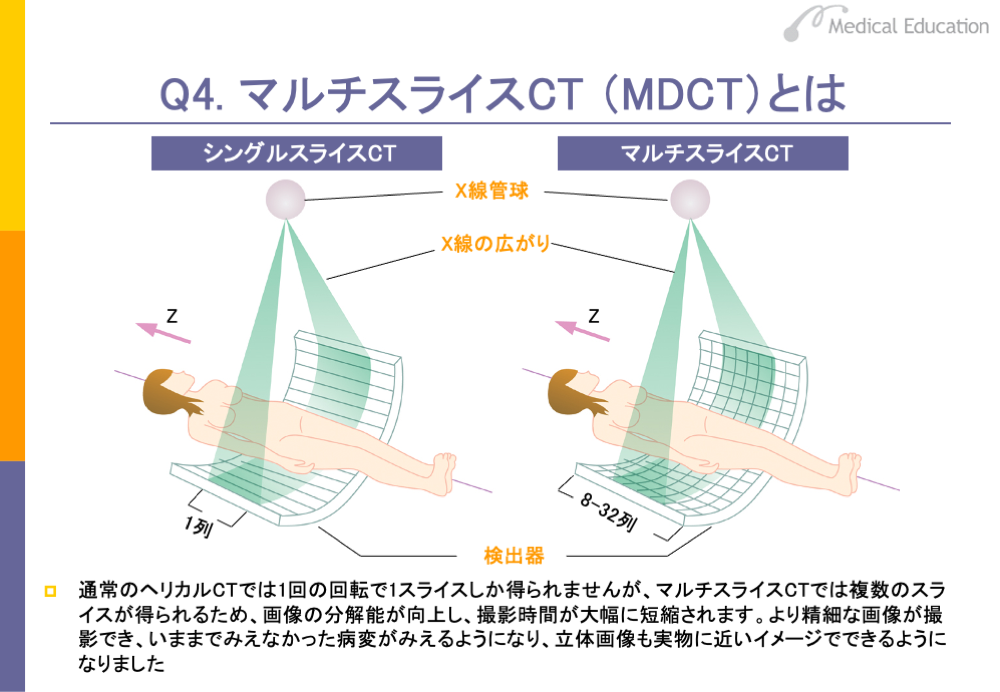
最新のCTには、 マルチスライスCT(MDCT )というものがあります。従来のCT(ヘリカルCT)ではⅩ線を検出する素子(detector)が1つしかありませんでしたが、マルチスライスCT は、スライド右のように素子を複数並べてCT撮影を行うものです。最近では64の素子を用いたものがあります。
マルチスライスCTの利点は、1㎜以下のスライスの検査を10秒ほどで行うことができる点です。その結果、非常に微小ながんでもみつけることができるようになりました。また、スキャンの時間が短いので、肺がんなどの場合、1回呼吸を止めるだけですべてのスキャンが終わります。マルチスライスCTが用いられるようになって、肺がんでは、非常に小さながんがみつかるようになり、治療成績の向上が期待されています。
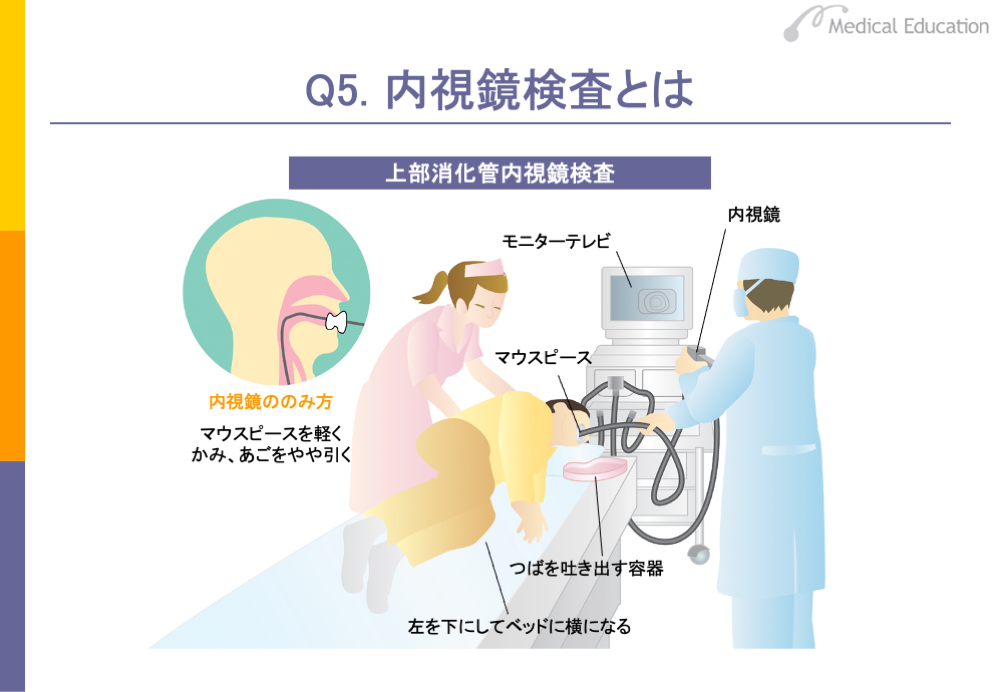
内視鏡検査とは、先端に小型カメラ (CCD) またはレンズを内蔵した太さ1cm程の細長い管を口、鼻あるいは肛門より挿入し、気管支、食道、胃、十二指腸や大腸の内部を観察し、時には治療を行うものです。消化管や肺のがんで必須の検査となっています。
上部消化管とは食道・胃・十二指腸を指します。スライドのように口または鼻から内視鏡を挿入し、これらの部位を一連の検査で観察します。昔から「胃カメラ」と言われてきたものです。

最新の内視鏡には、拡大内視鏡と超音波内視鏡があります。拡大内視鏡は、顕微鏡でしかみえないような微細なものを、一方、超音波内視鏡は超音波装置と内視鏡を組み合わせたもので、がんがどの深さまで達しているかなどをみることができます。がんが粘膜層にとどまっている場合は、その場で切除するなど、最近は内視鏡による診断だけでなく、その場で治療をするということが行われています。
また、小腸の内視鏡検査もめざましく進歩し、カプセル内視鏡とダブルバルーン内視鏡では、従来の内視鏡の欠点である腸を引き伸ばすことから起こる激しい痛み、小腸内に50cm~1m入ったところで先に進まないなどの点を改善しています。
カプセル内視鏡は、薬と同じように少量の水とともにのみ込み、消化管内部を蠕動運動によって移動し、体外に排出されるまで1秒当たり2枚の画像を6~8時間撮影し、体外に送信します。体への負担は少ない半面、見たい部位に誘導できない、組織の採取やポリープ切除ができない、使い捨てで費用が高い、などが課題です。
一方、ダブルバルーン内視鏡は、6~7mと長く、体の内壁に固定されず蛇行している小腸を2つの風船状のバルーンを使って、内視鏡が小腸の壁に当たらないように進むことができるようにしたものです。ダブルバルーン内視鏡は処置や治療を行えますが、カプセル内視鏡に比べて体への負担は大きく、検査には1時間半程度かかります。
従来の内視鏡と違い小腸の病変をみることができるというメリットがあります。ただし、通常の内視鏡では先端から生理食塩水を出して患部を洗ってみるため、非常にきれいな写真が撮れるのに対して、カプセル内視鏡では水が出せないためきれいな写真が得られないというデメリットがあります。
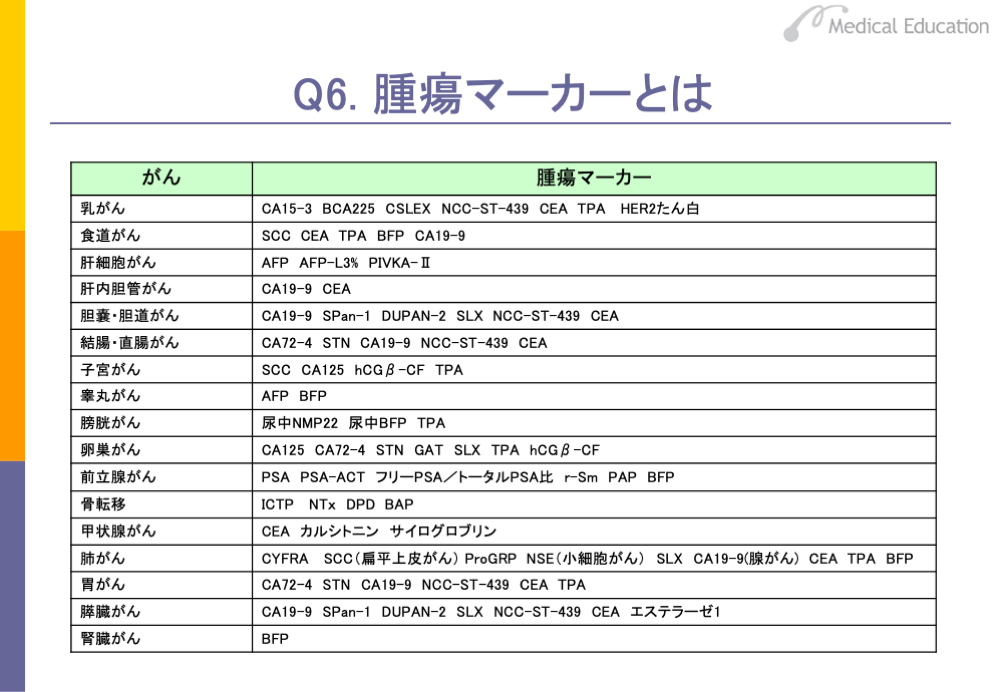
腫瘍マーカーとは、がんにより産生される特殊な物質で、血液や尿などの排出物中から検出できる物質をいいます。血液や尿などで調べることができることから、患者さんにとって非常に侵襲が少なく負担が少ない検査法です。臓器ごとに、それぞれ使うマーカーが異なります。
欠点は、かなり進行したがんでないと、腫瘍マーカーの値が上昇しないため、早期診断には役に立たないことです。ただし、前立腺がんは例外で、腫瘍マーカー
であるPSA(前立腺特異抗原)の値は、早期がんの段階でも上昇してきます。
このような腫瘍マーカーの性格から、腫瘍マーカーは、がんの補助的診断、組織型の鑑別診断、進行度などに関する情報として用いられているほか、治療がどの程度成功しているか、あるいは再発を起こしているかどうかを診断するときに用います。




