この講義で伝えたいこと
あなたが担当する製品は、妊婦に使用することはできますか。使用の際の注意点はありますか。
添付文書において、小児や高齢者、腎・肝機能障害を有する患者と同様に、妊婦は「特定の背景を有する患者」であることは、すべてのMRが認識していることでしょう。しかし、妊娠すると母体にどのような生理学的変化が生じ、どのように薬物動態が変化するかなど、妊婦についての知識をどれだけ持っているでしょうか。
この講義を通して、特定の背景を有する患者である「妊婦」に必要な薬学的対応を理解し、積極的にリスク最小化活動に取り組みましょう。
本編の前に
本編をはじめる前に、独自に行ったアンケート調査の結果を紹介します。
妊娠中の薬の服用に関するアンケート
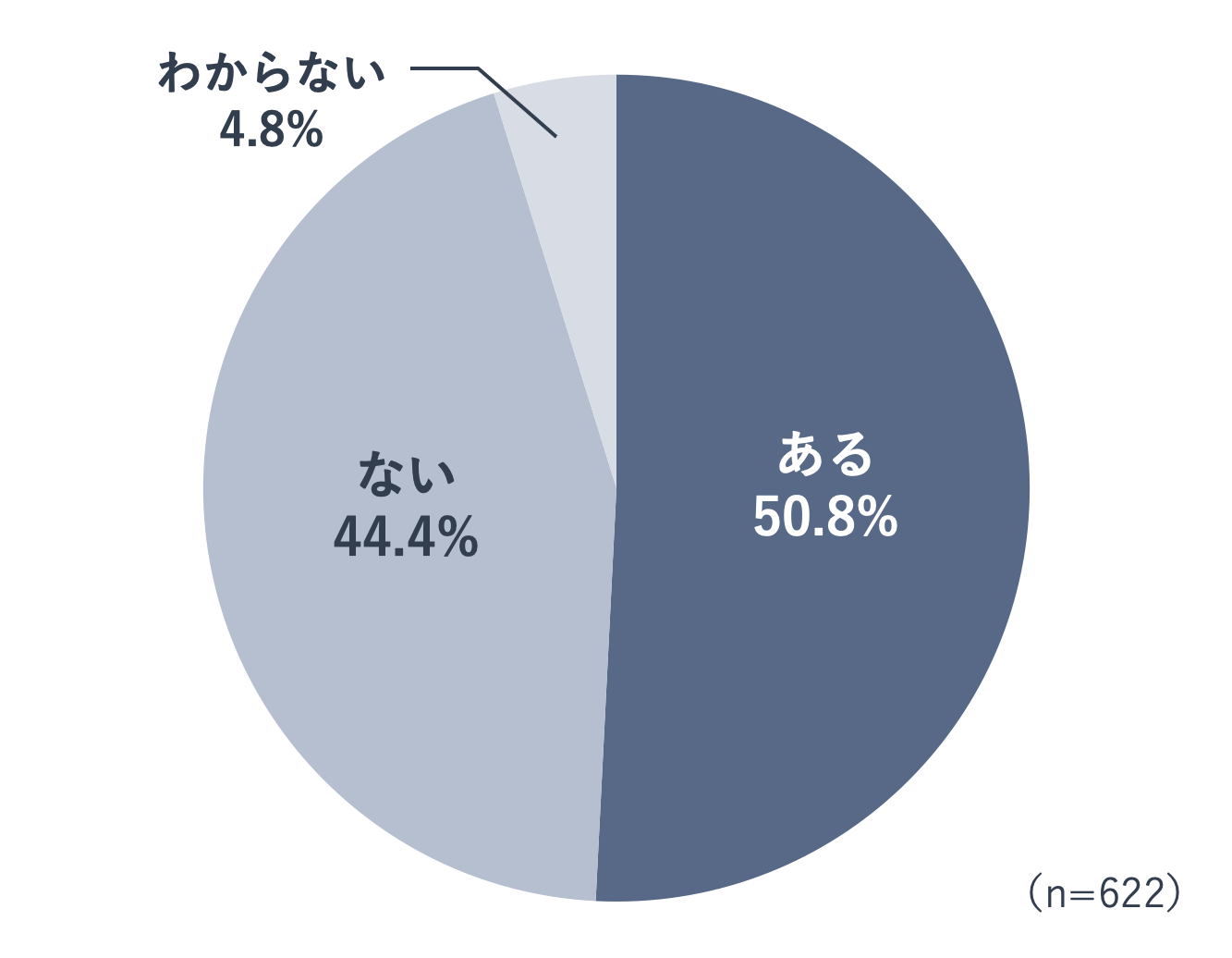
妊娠を経験したことがある20歳以上の女性に、「妊娠中の薬の服用について医師や薬剤師に相談したことがありますか。」と質問したところ、50.8%の人が「ある」と回答しました。
厚生労働省が妊産婦を対象に実施したアンケート調査では、妊娠中の健康管理で困ったことや不安に思ったこととして、「食事・栄養について」(54.2%)、「インフルエンザの予防接種などの感染症予防について」(51.0%)をおさえて、最も多くの人が回答に挙げたのは「飲んでよい薬かどうか」(58.2%)でした。
これらのアンケート結果からは、妊娠中の自身とお腹のこどもの健康のために、薬に対する妊婦の関心の高さ、不安の大きさを感じることができます。
【参考】厚生労働省「妊産婦の医療や健康管理等に関する調査」<結果概要>
妊娠によるからだの変化と薬物動態の変化
ここから、講義の本編をはじめます。まずは、妊娠によって起こるからだの変化と薬物動態の変化についてみていきます。
胎児の発生・発育と薬の影響
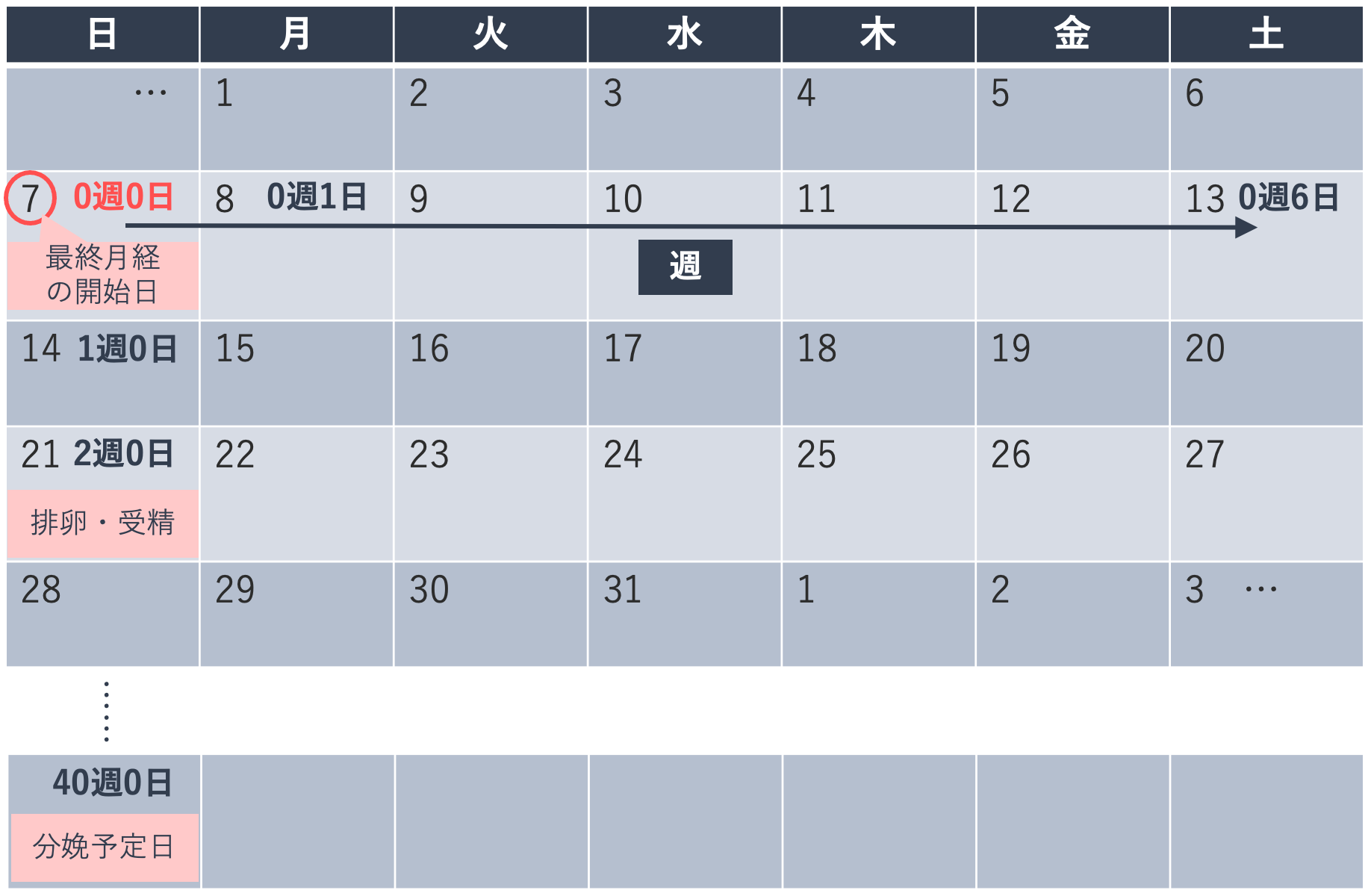
妊娠の時期は週数で表します。妊娠週数は月経周期が28日型を基準に計算し、最終月経の開始日を0週0日として、0から6日を1週として数えます。最終月経の開始日の次の日は0週1日、0週6日の次は1週0日となります。2週0日を排卵・受精、40週0日(280日目)を分娩予定日としますが、実際の月経周期は28日型とは限らないため、妊娠初期に超音波検査で胎児の大きさを測定して妊娠週数や分娩予定日を確定します。
【参考】「産婦人科診療ガイドライン―産科編2020」には、近年は、妊娠初期に計測されたCRL(胎児頭殿長:頭からお尻までの長さ) により計算される妊娠週数は、最終月経からの計算と比べ正確であると考えられており、米国産科婦人科学会(ACOG:American College of Obstetricians and Gynecologists)のガイドラインでも、分娩予定日は超音波計測値をもとに決めることを推奨しているとの記載がある。
妊娠時期は、妊娠14週未満を妊娠初期、妊娠14週から28週未満を妊娠中期、妊娠28週以降を妊娠後期と分類し、胎児の発育過程からは、受精から約2週間を着床前期、妊娠4週から9週未満を胎芽期、妊娠10週以降出生までを胎児期とします。
下の図は、妊娠周期と胎児の発生・発育に薬が影響を与える時期を示したものです。
妊娠3週末までは無影響期と呼ばれ、all or noneの法則が成り立つと言われています。この時期に接合子の細胞がダメージを受けると、胎芽死亡を引き起こし流産となるか、ダメージは修復され正常発生が継続するかのどちらかとされています。この時期に母体が医薬品を服用したとしても、妊娠が継続しているのであれば、胎児に影響はないと考えられます。ただし、長期間体内に蓄積する薬物ではこれに該当しない可能性があります。
妊娠4週から7週末までは絶対過敏期と呼ばれ、胎児が薬物の影響を最も受ける時期です。さまざまな器官が形成される時期のため、催奇形性のリスクが高くなります。月経が始まらず産婦人科を受診し妊娠が判明するのはこの時期であることが多いです。
妊娠8週から15週末までは相対過敏期と呼ばれます。胎児の重要な器官の形成は終了し、外性器が分化、口蓋が形成される時期です。絶対過敏期より薬物の影響は小さくなりますが、奇形のリスクはあります。
妊娠16週以降は潜在過敏期と呼ばれます。催奇形性のリスクは低下しますが、胎児毒性や分娩に影響する可能性があります。
薬物の胎児への影響は、催奇形性と胎児毒性に分けて考えられます。ヒトの出生では、3~5%に先天性の形態異常が生じるとされ、これをベースラインリスクと呼びますが、催奇形性がある薬物はこれを上回る頻度で胎児に奇形を生じさせます。対して胎児毒性とは、胎児の発育や機能に影響を及ぼすことをいいます。
薬による胎児への影響
- 催奇形性
薬物が生物の発生段階で奇形を生じさせる性質のこと。またその作用。催奇形性がある薬物はベースラインリスクを上回る頻度で胎児に奇形を生じさせる。 - 胎児毒性
胎児の発育や機能に影響を及ぼすこと
編集部作成
妊娠した母体の変化
妊娠中の母体は、妊娠を維持し、胎児の成長に対応して分娩に備えるため刻々と変化します。皮膚や体形、内部の器官や機能も変化します。
妊娠が成立すると胎盤の絨毛組織から産生されるヒト絨毛性ゴナドトロピン(hCG)の刺激により、胎盤からエストロゲンやプロゲステロンなどのホルモンが分泌され、生理学的な変化が生じます。血液、心血管、呼吸器、消化器、泌尿器、内分泌などさまざまな器官・機能に変化をきたし、分娩すると6~8週間かけて妊娠前の状態に戻ります。
妊娠により生理的変化が生じる器官および機能
- 血液
- 循環動態
- 呼吸機能
- 腎・尿路系
- 消化器
- 代謝
- 骨格・皮膚
編集部作成
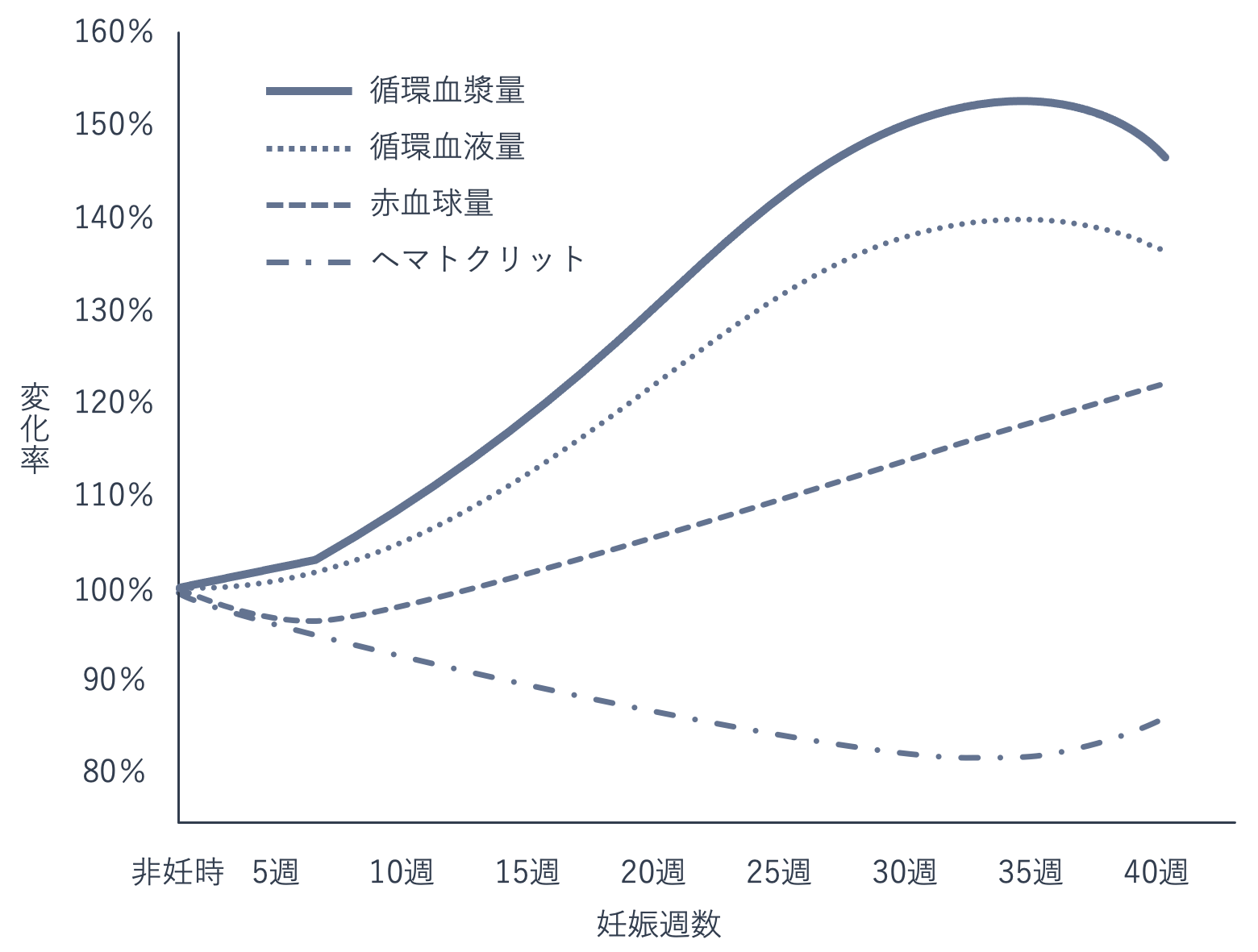
血液に関しては、母体の体重が増加するうえに、胎児に血液を供給する必要があるため、妊娠週数が進むにつれ循環赤血球量と循環血漿量が増加します。循環赤血球量の増加よりも循環血漿量の増加が大きいため、ヘモグロビン値やヘマトクリット値(※)が低下します。白血球数は徐々に増加し、血小板数は減少することがあります。凝固系は亢進、線溶(※)系は抑制状態となります。
※ヘマトクリット値:血液に占める赤血球の割合、またはその検査。貧血を判断するのに用いられる。(厚生労働省「e-ヘルスネット」引用)
※線溶:線維素溶解のこと。血液凝固系により形成された止血栓は、線溶系により分解、除去される。
心血管系では、心拍数と1回拍出量が増加するため、心拍出量も増加します。一方、血圧は軽度に低下します。分娩時には一過性に心拍数や血圧が上昇します。
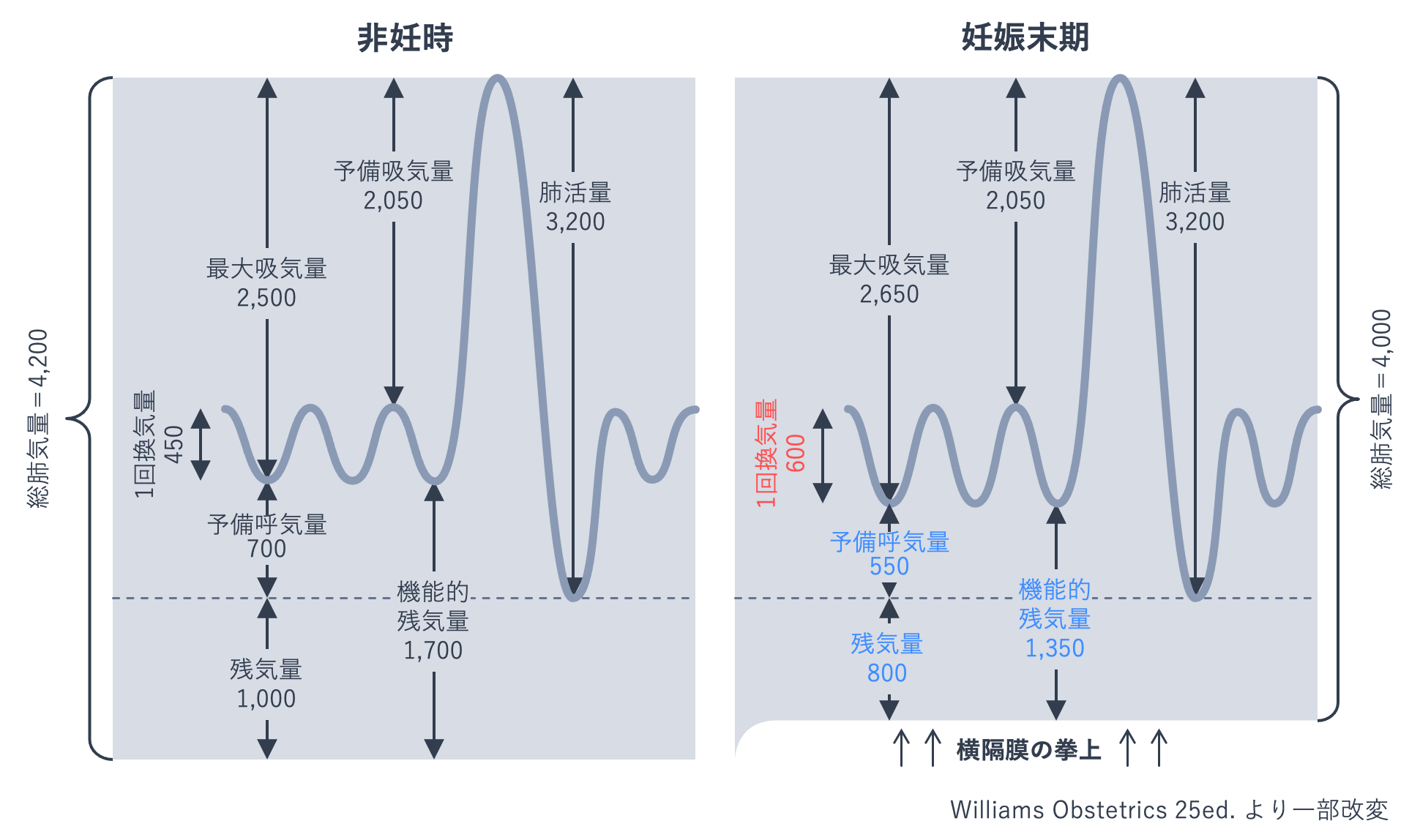
呼吸器系では、子宮の増大に伴い横隔膜が挙上するため、腹式呼吸に変化します。予備呼気量と残気量、その合計である機能的残気量は減少し、1回換気量は増加します。酸素消費量は増加しますが、1回換気量の増加などに伴い全酸素運搬容積が増加し、酸素摂取量が酸素需要を上回ります。
【参考】「MRテキスト2018 疾病と治療 基礎」より引用
・1回換気量:安静時呼吸において1回の呼吸運動で肺に出入りする空気量。
・予備吸気量:安静時吸気の終了からさらに追加吸入可能な最大空気量。
・予備呼気量:安静時呼気の終了からさらに呼出できる最大空気量。
・機能的残気量:安静時呼気の終了時に肺内に残る空気量。機能的残気量=予備呼気量+残気量。
泌尿器系においては、循環血漿量と心拍出量の増加により、腎血漿流量(RPF)、糸球体濾過量(GFR)が増加し、尿量が増えます。腎機能が亢進することにより血中尿素窒素(BUN)、血清クレアチニン(Cr)、尿酸の値は低下します。尿量の増加に加えて、子宮が増大することによる膀胱圧迫により、頻尿傾向になります。
妊娠により腎臓に生じる生理的な変化と検査値の変化
| 変化 | 変化内容(非妊時との比較) |
|---|---|
| 腎容積 | 約30%増大 |
| 腎血漿流量(RPF) | 妊娠初期、中期を通じて50%増加 |
| 糸球体濾過量(GFR) | 妊娠4週で20%増加 9週で45%増加 満期には 40%増加 |
| 尿素窒素(BUN) | 低下 |
| 血清クレアチニン(Cr) | 低下 |
| 尿酸 | 妊娠初期にはやや低下 妊娠末期にかけて上昇する傾向 |
編集部作成(参考:「腎疾患患者の妊娠診療ガイドライン2017」など)
消化器系では、消化器平滑筋が弛緩することと子宮の増大により胃が圧迫されることによって、消化管の蠕動運動が抑制されます。さらに下部食道括約筋の筋力が低下します。そのため胃内容排泄遅延や胃酸の逆流が生じやすくなります。
代謝、内分泌系においても変化があり、血中の遊離脂肪酸(FFA)やトリグリセリド(TG)、コレステロールなどの脂質の増加、インスリン抵抗性の増大、甲状腺ホルモンの変化などをきたします。
妊娠による代謝・内分泌系への影響
- 脂質代謝
血中の遊離脂肪酸(FFA)、トリグリセリド(TG)、コレステロールなどの脂質の増加 - 糖代謝
インスリン抵抗性の増大 - 甲状腺ホルモン
血中濃度上昇
編集部作成
【参考】 妊娠し胎盤が形成されると、胎盤からはプロゲステロン、プロラクチン、コルチゾール、胎盤性ラクトゲンなどのインスリン拮抗ホルモンが分泌される。それらにより、インスリン抵抗性が増大する。妊娠中は甲状腺ホルモン需要量が非妊娠時の約1.5倍に増加する。妊娠中に産生される絨毛性ゴナドトロピン(hCG)は甲状腺機能に影響を与え、甲状腺ホルモンの血中濃度は上昇する。
妊娠による薬物動態の変化
妊娠中の母体には生理学的な変化が生じているため、薬物動態は妊娠していない時とは異なります。
消化管の蠕動運動が抑制されることにより、薬物の吸収が遅れ、薬効の発現が遅延することがあります。循環血漿量の増加により血漿蛋白濃度が低下するため、遊離型薬物の割合が増加します。腎機能が亢進するため、薬物の腎排泄が増加します。妊娠すると薬物の血中濃度は低下する傾向があります。
妊娠中の生理学的変化による薬物動態への主な影響
| 妊娠に伴う生理学的変化 | 一般的な薬物動態の変化 | |
|---|---|---|
| 吸収 | 消化管蠕動運動の抑制 胃内pH上昇 |
薬効発現の遅延 |
| 分布 | 循環血漿量増加 体内水分量増加 |
分布容量増加 |
| 血漿中アルブミン濃度低下 | 遊離型薬物濃度増加 | |
| 代謝 | CYP1A2活性低下 | 血中半減期延長 |
| 排泄 | 腎血漿流量増加 糸球体濾過率増加 |
腎クリアランス増加 |
編集部作成
【参考】 血漿中アルブミン(※)濃度の低下による薬物のタンパク結合率の低下は、総血中濃度に比して遊離型の濃度上昇、つまり薬効が強く出ることになる。
※アルブミン:血漿タンパクの中で最も量が多いタンパク質。血管中の血液量や体内水分量を調整する働きのほか、脂肪酸、ホルモン、薬物などの物質と結合して運搬する働きがある。
妊婦の合併症とその影響
ここからは、妊婦の合併症とその影響についてみていきます。
妊婦の年齢とリスク
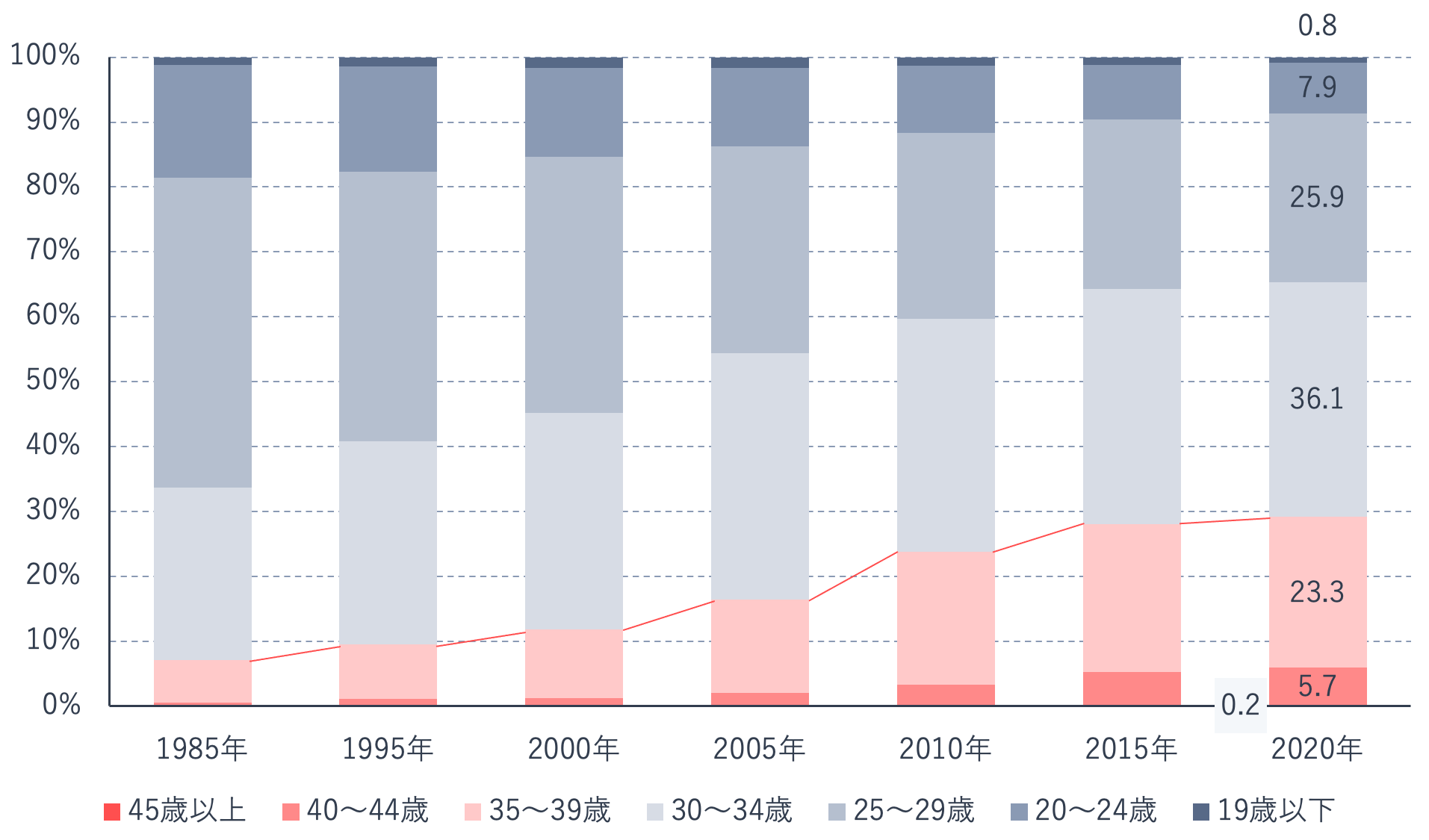
厚生労働省の報告によると、近年35歳以降に出産する割合が徐々に大きくなり、2015年頃からは約3割を占めています。
ライフスタイルの多様化や晩婚化などを背景に、高齢での妊娠・出産の割合が増える一方で、高齢で妊娠・出産することに対しては、合併症、児の染色体異常、母体だけでなく児の死亡率の増加が報告されるなど、さまざまなリスクが指摘されています。
妊婦の合併症には、妊娠に伴う合併症である産科合併症と、妊娠に関係なく発症する疾患である偶発合併症があります。
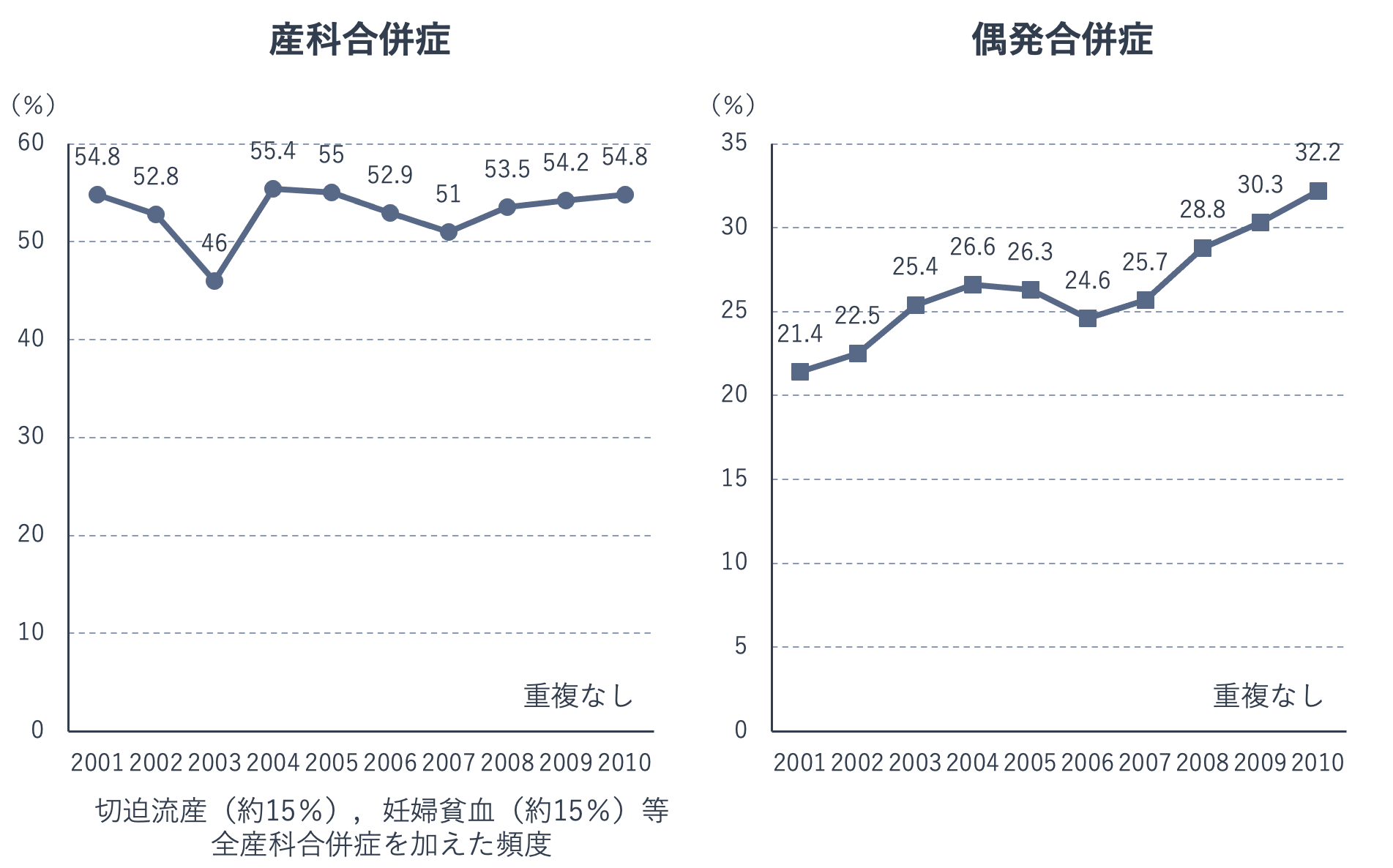
少し古い資料になりますが、下の図は、合併症の頻度年次推移を示したものです。産科合併症は全妊産婦の5割程度に発生しています。その発生頻度は横ばいですが、産科合併症は母体の年齢が上昇するとそのリスクは高くなります。一方、偶発合併症の発生頻度は増加しています。
偶発合併症は年齢の上昇に伴い高血圧や2型糖尿病、肥満などを抱える妊婦が増えるため、そのリスクは高くなります。偶発合併症はさらに合併症を引き起こす可能性があります。たとえば、妊娠糖尿病では母体が高血糖であることが胎児にも影響を及ぼし、流産や早産、妊娠高血圧症候群、羊水過多、巨大児、新生児低血糖などを生じることがあります。
頻度の高い合併症
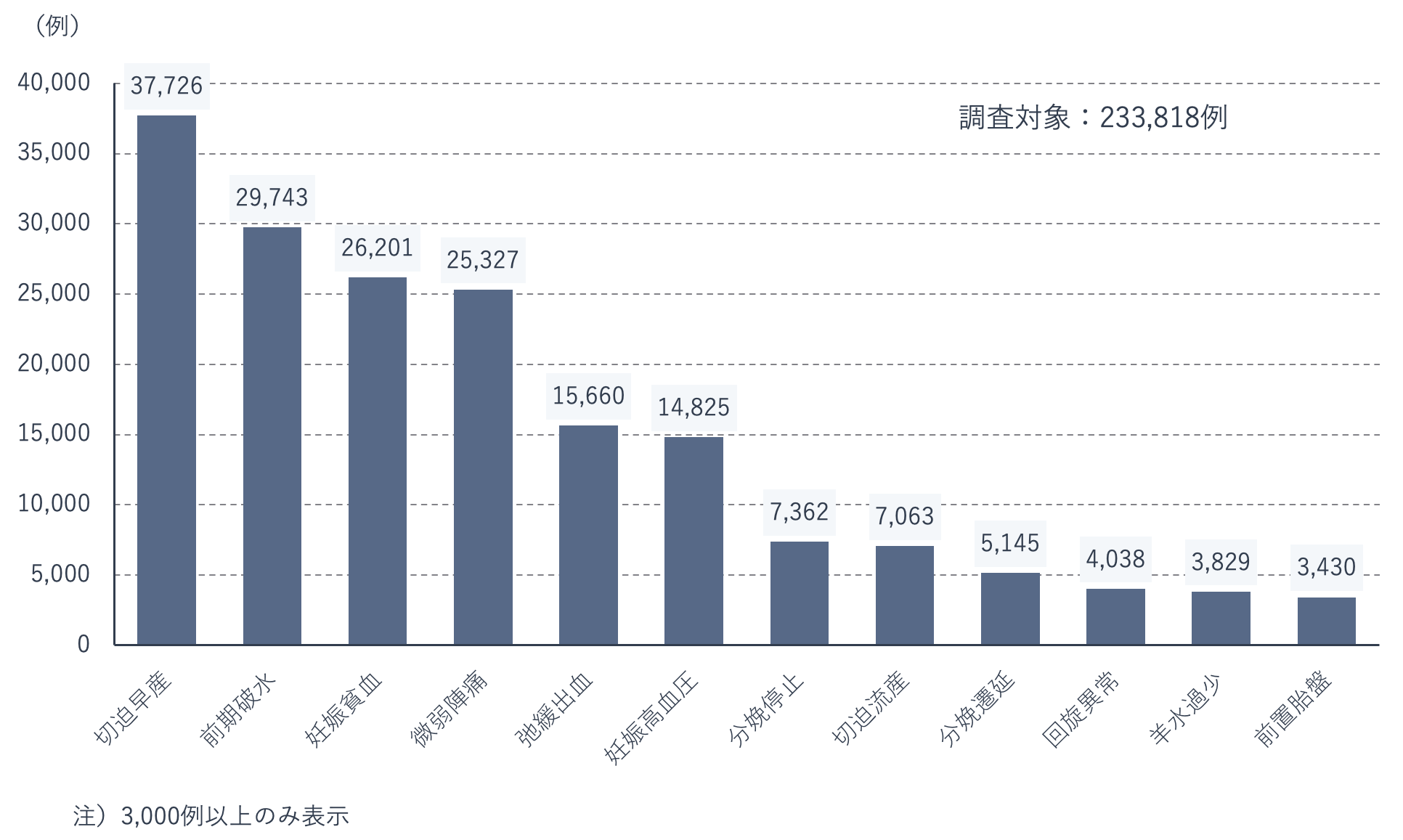
日本産科婦人科学会周産期登録事業の令和2年度報告(2019年周産期登録データ)によると、産科合併症の内訳としては、近年は切迫早産が最も多く、次いで前期破水、妊娠貧血、微弱陣痛、弛緩出血、妊娠高血圧症の順に続きます。
こちらは同報告による偶発合併症の内訳です。妊娠糖尿病(GDM)が最も多く、次いで子宮筋腫、甲状腺疾患、精神疾患が続いています。
偶発合併症で最も高い頻度でみられる妊娠糖尿病(GDM)について整理しておきます。
妊娠糖尿病とは、妊娠中にはじめて発見された糖代謝異常をいいます。妊娠前から糖尿病と診断されている場合は、糖尿病合併妊娠といいます。
妊娠前に見逃されていた糖尿病、妊娠中の糖代謝の変化の影響を受けた糖代謝異常、妊娠中に発症した1型糖尿病は、「妊娠中の明らかな糖尿病」と分類されます。妊娠中の明らかな糖尿病は、妊娠糖尿病より重度の状態であるため、より厳密な血糖管理が必要です。
これらの糖代謝異常合併症は、妊娠後期に子宮内胎児死亡の危険が高まるため、ハイリスク妊娠(※)の一因となります。
※ハイリスク妊娠:母児のいずれかまたは両者に重大な予後不良が予想される妊娠。
妊娠中の糖代謝異常
- 妊娠糖尿病
75gOGTT において次の基準の1点以上を満たした場合に診断する。
①空腹時血糖値 ≧92mg/dL (5.1mmol/L)
②1時間値 ≧180mg/dL (10.0mmol/L)
③2時間値 ≧153mg/dL (8.5mmol/L) - 妊娠中の明らかな糖尿病
妊娠前に見逃されていた糖尿病と、妊娠中の糖代謝の変化の影響を受けた糖代謝異常、および妊娠中に発症した 1 型糖尿病が含まれる。
以下のいずれかを満たした場合に診断する。
①空腹時血糖値 ≧126mg/dL
②HbA1c 値 ≧6.5% - 糖尿病合併妊娠
①妊娠前にすでに診断されている糖尿病
②確実な糖尿病網膜症があるもの
「産婦人科診療ガイドライン―産科編2020」 より編集部作成
妊婦の約20人に1人の割合で起こるといわれている妊娠高血圧症候群についても、整理しておきます。
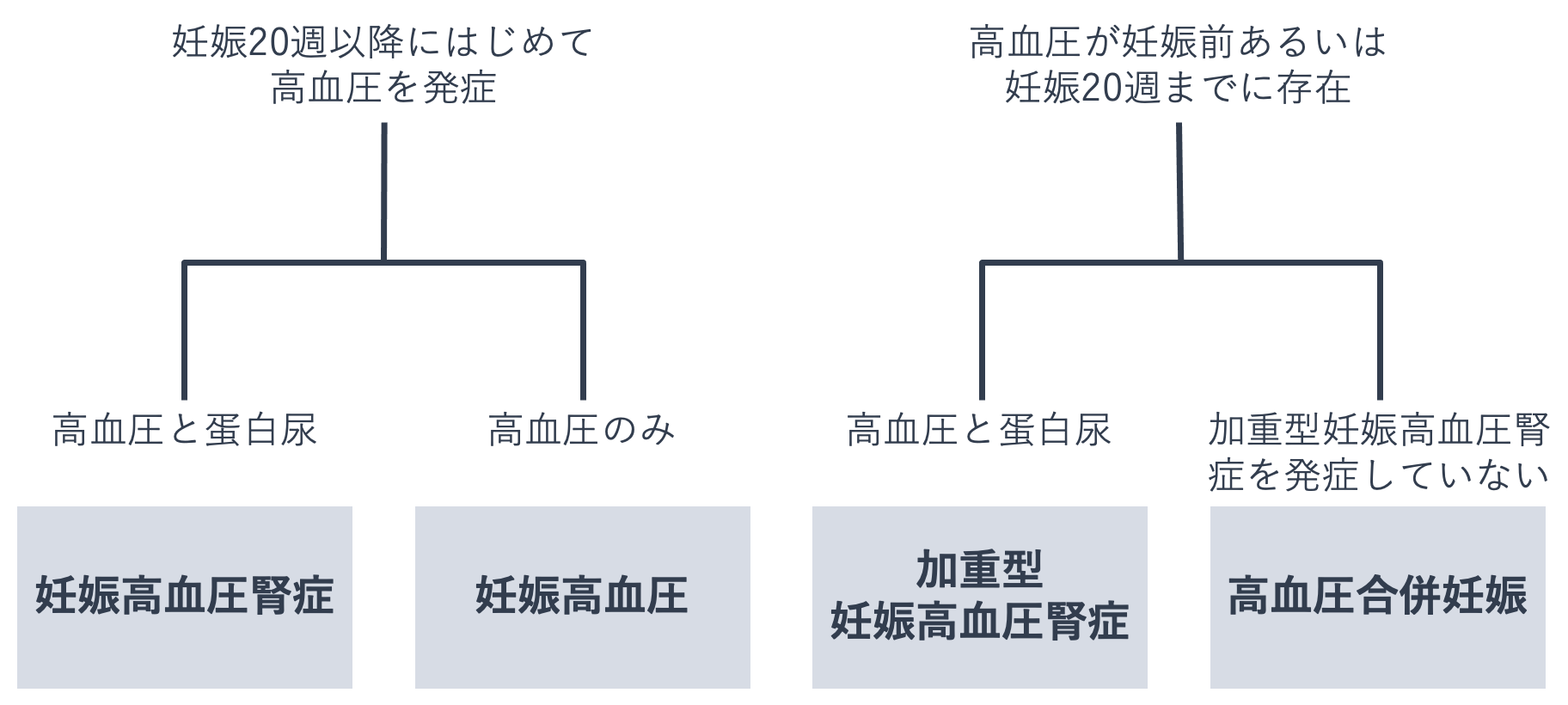
妊娠時に高血圧を認めた場合を妊娠高血圧症候群といいます。妊娠高血圧症候群は、妊娠高血圧腎症、妊娠高血圧、加重型妊娠高血圧腎症、高血圧合併妊娠に分類されます。
妊娠高血圧腎症は妊娠20週以降に高血圧と蛋白尿を認める場合、妊娠高血圧症は妊娠20週以降に高血圧のみ発症する場合、高血圧合併妊娠は妊娠前あるいは妊娠20週までに高血圧を認め、加重型妊娠高血圧腎症を発症していない場合に分類されます。
妊娠高血圧症候群が重症化すると、HELLP症候群(※)、痙攣発作(子癇)、脳出血などを引き起こすことがあります。また、胎児の発育不全や機能不全などを引き起こすこともあり、妊娠高血圧症候群はハイリスク妊娠の一因となります。
※HELLP症候群:妊娠中・分娩時・産褥時に溶血所見、肝機能障害、血小板数減少を同時に伴い、他の偶発合併症によるものではないものをいう。
医薬品開発の視点からみる妊婦
ここからは、妊婦を医薬品開発の視点からみていきます。
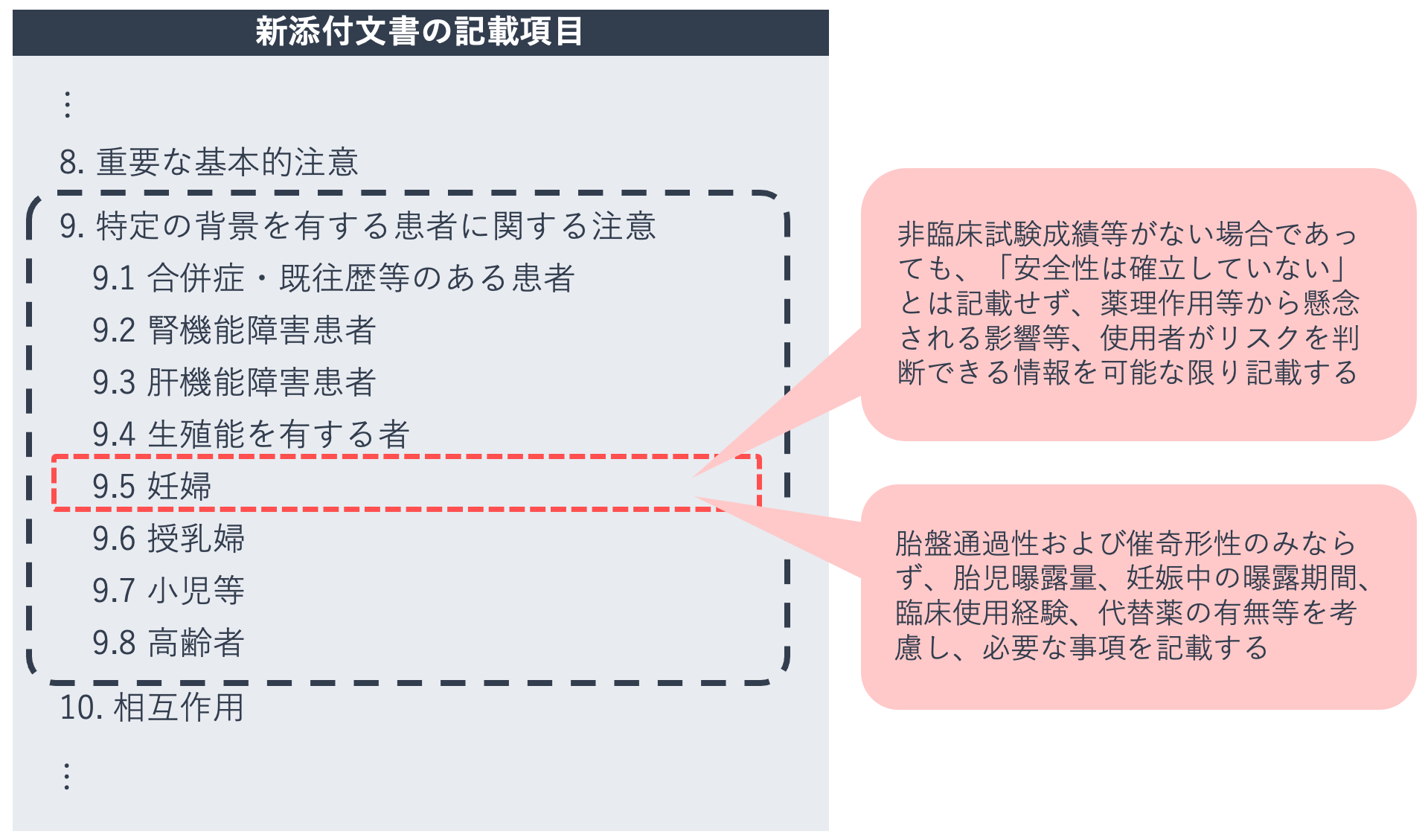
添付文書の妊婦に関する記載
倫理的観点から妊婦・授乳婦が治験の試験対象に組み入れられることはありません。そのため、新規医薬品の承認直後には、妊婦・授乳婦への使用に関する注意情報は生殖発生毒性試験の結果を参照して確認します。
医療用医薬品の添付文書(新記載要領)では、妊婦・授乳婦に関する情報は「9.特定の背景を有する患者に関する注意」の「9.5妊婦」「9.6授乳婦」に記され、生殖発生毒性試験の結果が記載されていることがあります。非臨床試験で妊娠、胎児および出生児への影響が認められていないものであって、薬理作用からも影響が懸念されないものに関しては、「妊婦」の項目は記載されず欠番となります。
【参考】2019年4月1日時点で既に承認されている医薬品の添付文書については、2024年3月31日までに新記載要領に基づいた改訂を行うこととされている。そのため現時点では旧記載要領に基づく添付文書と混在している。旧記載要領では、妊婦に関する情報は「妊婦・産婦・授乳婦等への投与」の項目に記載される。
妊婦に対する注意事項は、「投与しないこと」、「投与しないことが望ましい」、「治療上の有益性が危険性を上回ると判断される場合にのみ投与すること」の3つを基本として記載されます。
それぞれの記載の目安は下の表に示したとおりです。
妊婦に対する注意事項の記載の目安
| 表記 | 記載内容 |
|---|---|
| 【投与しないこと】 | 以下のいずれかに該当し、かつ、妊婦の治療上の有益性を考慮しても、投与すべきでないもの
|
| 【投与しないことが望ましい】 |
|
| 【治療上の有益性が危険性を上回ると判断される場合にのみ投与すること】 |
|
編集部作成(参照:「医療用医薬品の添付文書等の記載要領に関する質疑応答集(Q&A)について」)
インタビューフォームの生殖発生毒性試験に関する記載
インタビューフォームには生殖発生毒性試験の概要と結果が記載されています。
生殖発生毒性試験は、哺乳類の生殖発生に対する医薬品の影響を明らかにして、ヒトでのリスク評価に役立てるために非臨床で行われる試験です。生殖発生ステージにおける評価時期により3種類の試験(受胎能及び着床までの初期胚発生に関する試験[FEED試験]、2種の動物種を用いた胚・胎児発生に関する試験[EFD試験]、出生前及び出生後の発生並びに母体の機能に関する試験[PPND試験])に分類されます。
FEED試験では、雄動物および雌動物において交配前から交尾、着床に至るまでの被験薬物の投与による有害作用を検討します。着床以前の受精卵への薬物の影響はall or noneの法則に従うとされているため、FEED試験で示された毒性については妊娠が継続しているのであれば影響はないと考えることができます。
EFD試験は、胎児器官形成期の妊娠雌動物において、被験薬物の投与による母動物および胚・胎児の発生への有害作用を検出するために実施され、生殖発生毒性試験のなかで特に重視されます。胎児に奇形が生じていないか、胎児の死亡および発育遅延の可能性についても評価されます。
PPND試験は、着床から離乳までの間に母動物に被験薬物を投与したときの有害作用を検出し、妊娠中あるいは授乳中の雌動物および児の発生に対する影響を検討します。これにより授乳を介した薬物の児への影響が評価されます。
リスクと母体への利益のバランス
妊娠中は、胎児の発達・発育に悪い影響を与えることがないよう薬の服用は避けた方がよいと考えがちですが、必ずしもそうではありません。妊婦が慢性疾患を抱えている場合には、薬の服用を止めてしまうことで、疾患のコントロールが悪化し、胎児の発育に影響を及ぼすだけでなく、合併症が生じることがあります。妊婦は自身の体の変化や胎児への影響を踏まえつつ、より安全に薬と付き合わなければなりません。
下の表は、添付文書上「いわゆる禁忌」となっている医薬品のうち、特定の状況下では妊娠中であっても使用が検討される代表的な医薬品です。これらは、胎児への有害作用がヒトで証明されている医薬品ではなく、妊婦自身の健康維持のために必須である医薬品や、胎児への有害作用の可能性はあるものの特定の状況下ではそれを上回る母体への利益が考えられる医薬品です。
添付文書上いわゆる禁忌*の医薬品のうち特定の状況下では妊娠中であっても
インフォームドコンセントを得たうえで使用される代表的医薬品
| 医薬品 | 使用する状況 |
|---|---|
| ワルファリンカリウム(クマリン系抗凝血薬) |
|
| コルヒチン |
|
| イトラコナゾール(抗真菌薬) |
|
| 添付文書上いわゆる禁忌*の抗悪性腫瘍薬 |
|
| ニフェジピン(妊娠20週未満)、ニカルジピン塩酸塩(経口錠)、アムロジピンベシル酸塩 |
|
| アスピリン(妊娠28週以降、低用量) |
|
「産婦人科診療ガイドライン―産科編2020」 より作成
*「添付文書上いわゆる禁忌」とは:
1. 添付文書の記載要領(改定前)による記載として以下のいずれか。
1) 『使用上の注意』の『妊婦、産婦、授乳婦等への投与』項目に、「投与を避けること」「使用しないこと」「投与しない」「絶対に投与しないこと」いずれかの記載がある。
2)妊婦または妊娠している可能性のある婦人は禁忌、あるいは原則禁忌との追記がある。
2.添付文書の記載要領(改定後)による記載として以下のいずれかがある。
1)『禁忌(次の患者には投与しないこと)』の項目に妊婦が記載されている。
2) 『特定の背景を有する患者に関する注意』の『妊婦』の項目に「投与しないこと」との記載がある。
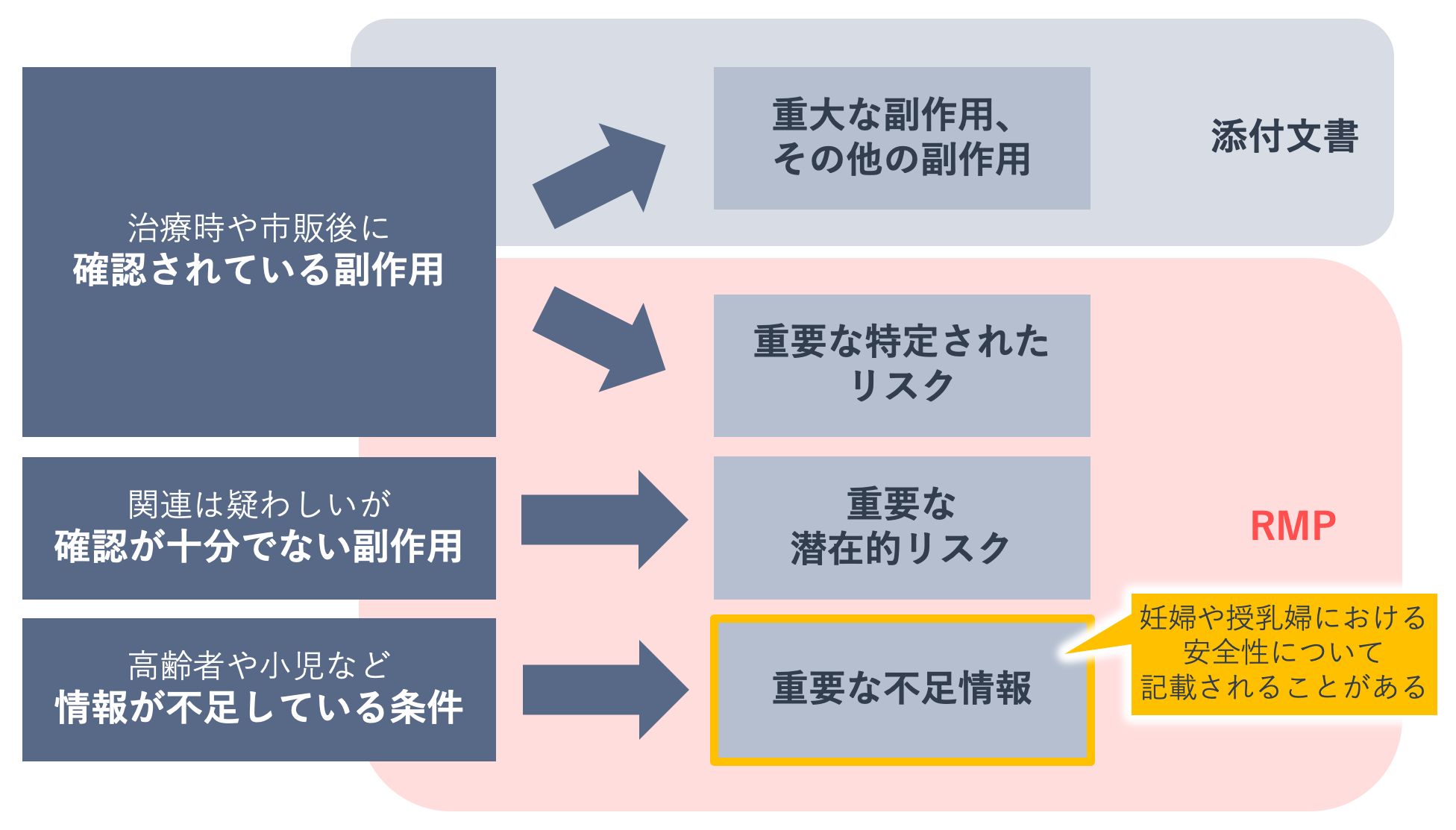
妊婦・授乳婦は治験の試験対象にならない、妊婦・授乳婦への投与事例が限られていることなどを背景に、医薬品の妊婦・授乳婦に関する安全性情報は不足しています。
2013年から適用が開始された医薬品リスク管理計画(Risk Management Plan:RMP)には、副作用などのリスクが整理され、不足している情報を得るための調査やリスクを最小化するための活動などがまとめて示されています。妊婦・授乳婦に関連するところでは、安全性検討事項の重要な不足情報に、妊婦や授乳婦に投与した際の安全性が挙げられ、医薬品安全性監視活動とリスク最小化活動が計画・実行されることがあります。
【参考例】エムガルティ皮下注120mgオートインジェクター、エムガルティ皮下注120mgシリンジに係る医薬品リスク管理計画書
RMPを利用して、医療機関からの情報収集と医療機関への情報提供を加速させ、その情報が医療現場で十分に活用されることは、患者である妊婦・授乳婦とその子供により安全な医療を提供することにつながります。
薬局薬剤師インタビュー
ここからは、薬局薬剤師が実際に体験したエピソードを紹介します。今回は、現在のコロナ禍中にあった妊婦さん(妊娠中期)とのやり取りです。
薬局でのエピソード
ある妊婦さんが、新型コロナウイルス感染症のワクチン接種後、副反応で37℃前半の発熱があるとのことで、ロキソニンを買いに来局されました。なぜロキソニンを希望されるのか尋ねたところ、妊婦さんは「ネットで調べたら、ロキソニンは妊娠中でも飲むことができて、コロナの重症化防止につながるとあったので。」と言います。最近はこのように、インターネット上の記事やSNSで得た情報をもとに医薬品を購入に来られる患者さんも少なくありません。
この妊婦さんには、まずはもう少し様子を見ること、薬を服用するのであれば妊婦に対してより安全性の高いアセトアミノフェン製剤にすること、発熱が続く場合は医師の診察を受けることをおすすめしました。
このように社会の状況が患者さんの行動に変化を生じさせることがあります。MRの情報提供も、社会情勢に応じた注意喚起を添えるなど、その時々で工夫する必要があります。

新型コロナウイルス感染症のワクチン接種後、副反応の発熱に対してロキソニンの購入を希望する妊婦さん
- 妊娠中でもロキソニンは飲むことができ、コロナの重症化防止につながるというネットの情報を信用
- 妊婦に対しより安全性の高いアセトアミノフェン製剤を勧め、症状が改善しない場合の受診勧奨を行った
- 社会の状況が患者さんの行動に変化を生じさせることがある
- MRの情報提供も、社会情勢に応じた注意喚起を添えるなど、その時々で工夫する必要がある
編集部取材より
薬局薬剤師さんのエピソードに登場した「ロキソニン」はNSAIDsです。NSAIDsの使用により胎児の腎機能障害および尿量減少とそれに伴う羊水過少症が生じた報告があることから、関係学会は、NSAIDsを妊婦に対して解熱鎮痛薬として投与する場合には必要最小限にとどめること、また適宜、羊水量を確認することが最近新たに添付文書に記載されたことを注意喚起しています。
NSAIDs添付文書改訂案
妊婦、産婦、授乳婦等への投与
妊婦(ただし、出産予定日12週以内の妊婦は除く)又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。投与する際には、必要最小限にとどめ、適宜羊水量を確認するなど慎重に投与すること。シクロオキシゲナーゼ阻害剤(経口剤、坐剤)を妊婦に使用し、胎児の腎機能障害及び尿量減少、それに伴う羊水過少症が起きたとの報告がある。
日本産科婦人科学会/日本産婦人科医会「NSAIDs 添付文書改訂に関する周知」資料 より
MRの皆さんへ
自身の担当製品の添付文書には、妊婦への使用についてどのような記載がされているか、改めて確認してください。「いわゆる禁忌」の記載にとどまっている場合は、医療者が使用リスクを判断できる情報を提供することを心掛けましょう。
そして、RMPの作成対象ではない製品についても、使用症例の収集といった安全性監視活動と、添付文書やインタビューフォームなど医薬品情報の基本資材の内容を確実に提供するといったリスク最小化活動を、担当する製品すべてで行う意識を持ちましょう。
MRの皆さんへ
- MRは、自身の担当製品の妊婦への使用について、医療者がリスクを判断できる情報を提供することを心掛けましょう。
- 使用症例の収集といった安全性監視活動と、添付文書やインタビューフォームなど医薬品情報の基本資材の内容を確実に提供するといったリスク最小化活動を、担当する製品すべてで行う意識を持ちましょう。
出典
- 日臨麻会誌 Vol.38,No.4, 533-538, 2018: 妊婦の生理学
- 日本循環器学会/日本産産科婦人科学会合同ガイドライン「心疾患患者の妊娠・出産の適応、管理に関するガイドライン(2018年改訂版)」
- 2020年2⽉6⽇ 公益社団法⼈⽇本産科婦⼈科学会「妊婦・産褥婦の新型コロナウイルスの感染予防対策について」
- 日本腎臓学会学術委員会編集「腎疾患患者の妊娠診療ガイドライン2017」
- 政府統計の総合窓口e-Stat 人口動態調査(確定数)2020年「母の年齢(5歳階級)別にみた年次別出生数・百分率及び出生率(女性人口千対)」
- 公益社団法人日本産科婦人科学会 周産期委員会 令和2年度報告
- 2019年3月15日 第2回妊産婦に対する保健・医療体制の在り方に関する検討会資料1
- 公益社団法人日本産科婦人科学会/公益社団法人日本産婦人科医会「産婦人科診療ガイドライン―産科編2020」
- 2017年6月8日 薬生発0608第1号
- 2019年1月17日 厚生労働省医薬・生活衛生局医薬安全対策課事務連絡
- 日本製薬工業協会 医薬品評価委員会 PV部会 継続課題対応チーム4「医薬品インタビューフォーム作成の手引き(改訂版)令和2年5月改訂(暫定版)」
- 2021年1月29日 薬生薬審発0129第8号「『医薬品の生殖発生毒性評価に係るガイドライン』について」
- PMDA「3分でわかる!RMP講座 第3版」
- 2021年3月8日 日本産科婦人科学会・日本産婦人科医会「NSAIDs 添付文書改訂に関する周知」資料2