- 編集部からのコメント
-
この記事は『Medical Education for MR 2017秋号』に掲載されたものを再掲したものです。
第2章で取りあげた費用対効果評価は、2019年4月より本格導入されています。医薬品では2019年度は6品目、2020年度は8品目、2021年度は11品目と、対象は徐々に拡大しています。
第3章で取りあげた最適使用推進ガイドラインも、2021年8月現在は11の医薬品で作成されています。
これら対象医薬品の拡大は、それだけ、画期的な新薬が生み出されているということでもあります。
【参照】
・国立保健医療科学院 保健医療経済評価研究センターウェブサイト「費用対効果評価の制度化以後(2019.4~)に選定された品目」
・PMDAウェブサイト「最適使用推進ガイドライン(医薬品)」
医薬品アクセスとは何か?
医薬品アクセスと制限
「アクセス」は、到達・手が届く・利用可能にするåという意味です。つまり「医薬品アクセス」とは、患者さんが医薬品を利用できる状態であることを指します。
医薬品は患者さんにとって大きな希望です。しかし、医薬品アクセスを制限する要素はたくさんあります。
医薬品アクセスの制限をグローバルな視点で捉えると、発展途上国や医療の未開の地において、医療提供体制や政情、製薬企業側の特許保護に関する問題などから、治療を必要とする患者さんに医薬品が届かないという大きな問題があります。
日本国内の視点では、ドラッグ・ラグの問題や、新規抗がん剤や肝炎治療剤といった高額薬剤(高薬価医薬品)の登場によるアクセス制限があります。
ドラッグ・ラグによるアクセス制限
日本は、国民皆保険制度の下、国民は誰でも最良の医療を受ける権利が保証されています。治療の一環である医薬品についても、患者が望む最良の医薬品が選択され、投与される権利を持っています。
これまでの医薬品アクセスの制限は、ドラッグ・ラグの問題が中心でした。ドラッグ・ラグとは、医薬品の承認の遅れ(ラグ)、つまり海外で使用できる薬が日本で使用できるようになるまでの遅れをいいます。
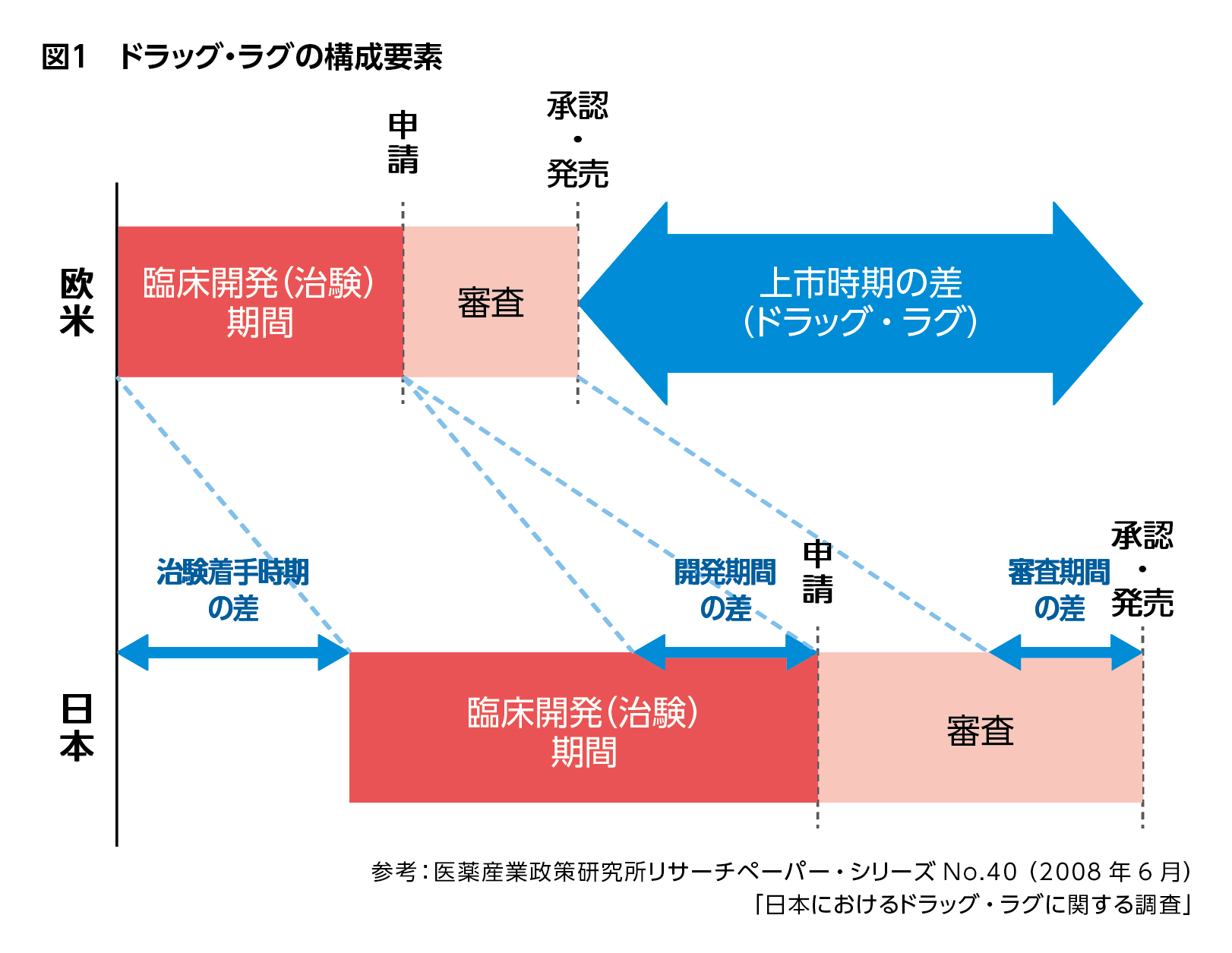
ドラッグ・ラグには大きく分けて2つの種類があります。ひとつは開発ラグと呼ばれる承認申請までの遅れです。もうひとつは審査ラグと呼ばれ、他国に比べて日本の審査期間が長くかかったことによる遅れです(図1)。
これらのラグにより、患者さんが望む医薬品を公的医療保険下で使用できないというアクセス制限が起こります。
ドラッグ・ラグを改善するため、薬価制度における「新薬創出・適応外薬解消等促進加算」の創設や、治験のスピード化、PMDAでの承認審査官増員といった対策が取られ、ドラッグ・ラグは解消に近づきつつあります。
また、2016年4月からは患者申出療養制度がスタートし、未承認薬についても従来よりスピーディーな手続きの下で使用できる道が開かれています。
医薬品アクセスの新たな課題
近年、医薬品アクセスの制限について新たな課題が出てきました。
医療保険財政に大きな影響を与える高額薬剤の登場により、超高齢社会を迎え枯渇する医療財源をいかに効率的に活用するか、医療にコストの視点をどうやって盛り込んでいくかが問われ、医療技術への費用対効果評価が議論されています。
必要とする患者さんに最良の医療技術や医薬品を滞りなく届けることこそが、製薬企業ならびに医療関係者の使命です。限りある財政のなか、最良のものを提供し続けるためには、さらに効率的な提供方法を考え続けなければなりません。
現在提供されている医療技術・医薬品が、それを求める患者さんにきちんと届いているか、また高額な医療技術・薬剤の増加などにより保険医療財政へ影響を及ぼしていないかなどを判断するために必要とされるのが、医療における費用対効果評価の考え方です。
医療に向けられるコストと効率化の視点
~費用対効果評価~
費用対効果評価導入の検討開始
費用対効果評価導入の検討が開始されたのは、医療技術も含め高薬価の医薬品の登場などによる医療保険財政への影響が懸念され、保険収載の可否や保険償還価格の判断材料としてその必要性が指摘されたことによります。
日本の医療保険制度は、安全性や有効性を中心に評価を行ってきましたが、今後は、従来の医療技術(医薬品も含む)よりも高額な費用を要する技術等、一定の基準により選定された医療技術を対象として、安全性・有効性といった効果のみならず、費用も考慮した評価を行うということです。
国による費用対効果評価の検討は、2012年度診療報酬改定に係る附帯意見を皮切りに、同年5月から中央社会保険医療協議会(以下、中医協)の費用対効果評価専門部会(以下、専門部会)でスタートしました。
費用対効果評価の現状
2016年度診療報酬改定では費用対効果評価が試行的に導入されました。保険医療財政への影響や革新性、有用性が大きい医薬品・医療機器を対象として13品目が選定され、うち医薬品では7品目が選定されています(表1)。これらの中には、医療保険財政に影響を与えかねないとして中医協で議論になっている高額薬剤も含まれます。
現在はまだ試行的導入ですが、本格的導入に向けて中医協専門部会で議論が続いています。
費用対効果評価と医薬品アクセス制限の関係
では、費用対効果評価の導入と医薬品アクセス制限にどのような関連があるのでしょうか。
例えばイギリスでは、国民医療サービスで提供する医療技術(医薬品を含む)の償還の可否決定の判断、また使用患者の制限の判断に、費用対効果評価を導入しています。そのため、抗がん剤や認知症治療薬などで、使用制限のために必要な薬物療法を受けられないとして、患者団体の抗議活動が起こりました。
このように、費用対効果評価を導入することで、保険償還されないことによる使用制限、承認から償還決定までに時間を要することによる時間的制限、採算割れ懸念による開発企業の新薬上市見合わせや市場からの撤退といった医薬品アクセス制限が起こることが懸念されます。
費用対効果評価の流れ
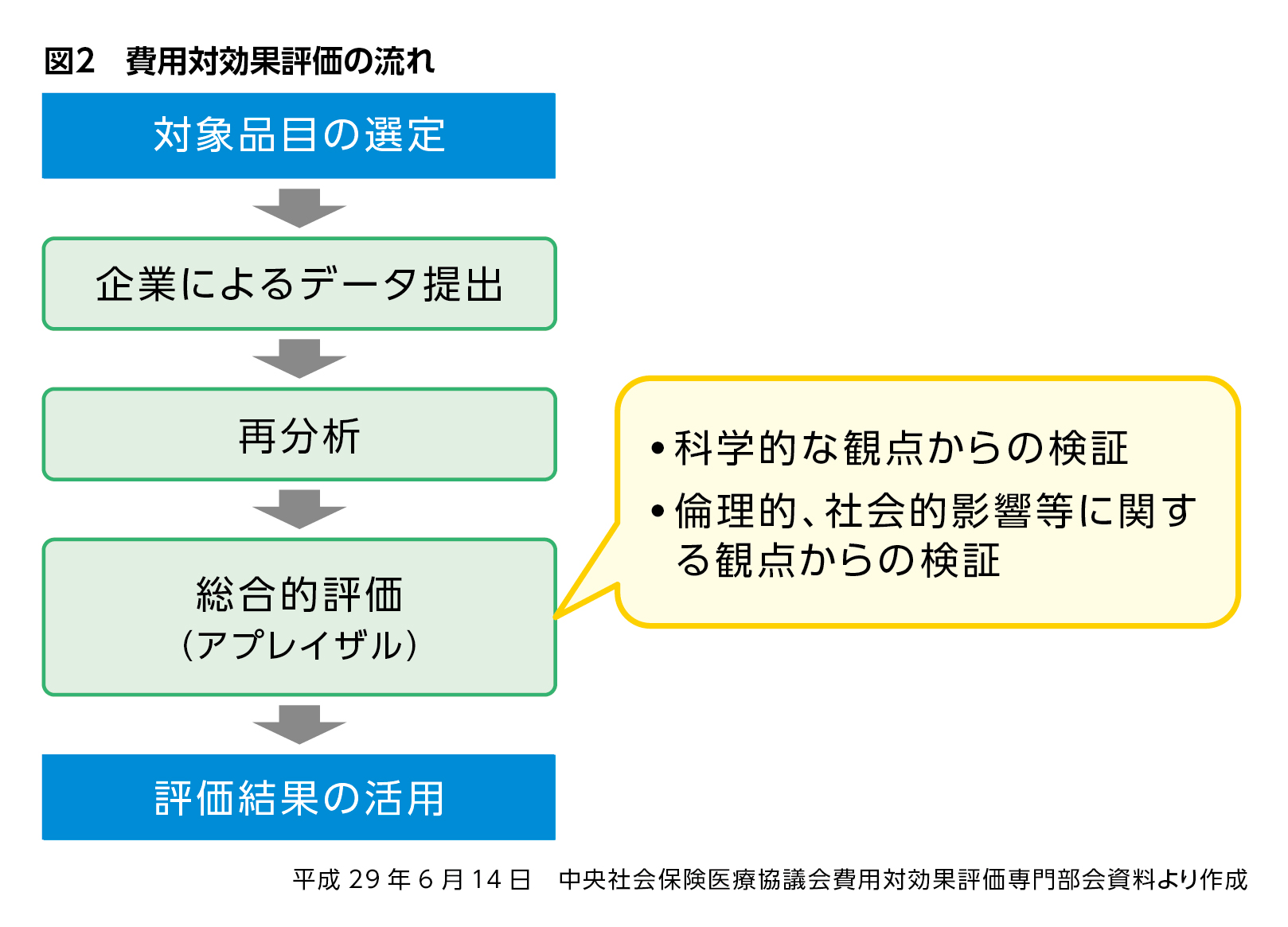
試行的導入に選定された対象品目は、製薬企業から「費用」と「効果」の分析データ提出を受け、外部専門家などから構成される専門機関において再分析が行われます。
さらに、中医協の下に設置される費用対効果評価専門組織で、分析結果の妥当性を科学的な観点および倫理的、社会的影響等に関する観点から検証を加えた総合的評価(アプレイザル)を行い、中医協での審議により評価結果に基づく価格調整が実施されることになります(図2)。
総合的評価の倫理的・社会的影響等の観点
2017年7月12日の専門部会ではこれまでの議論のまとめ案が出されていますが、総合的評価(アプレイザル)における倫理的・社会的影響等の観点での評価の際に考慮すべき要素については、引き続き検討が必要とされています。
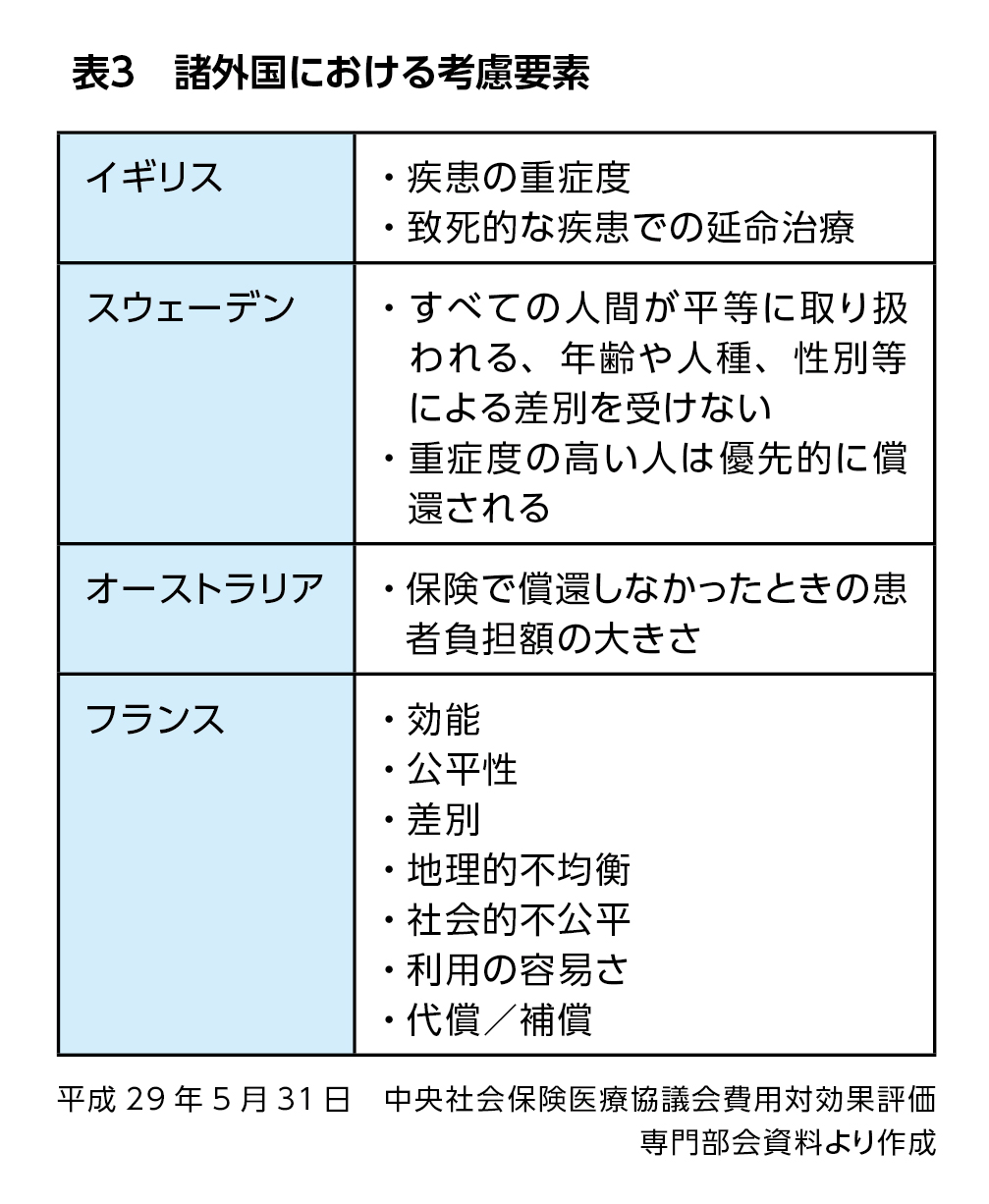
これまでの議論であがった考慮する要素の案では、感染症対策といった公衆衛生上の課題等があり(表2)、また、イギリスやフランス、スウェーデン、オーストラリアといった諸外国の考慮要素(表3)を参考にしながら、日本における総合評価のあり方を議論していくことになっています。
費用対効果の5段階評価
医薬品アクセスについては、患者自身が受けた診療への対価をどのように考えているかが大きな問題です。
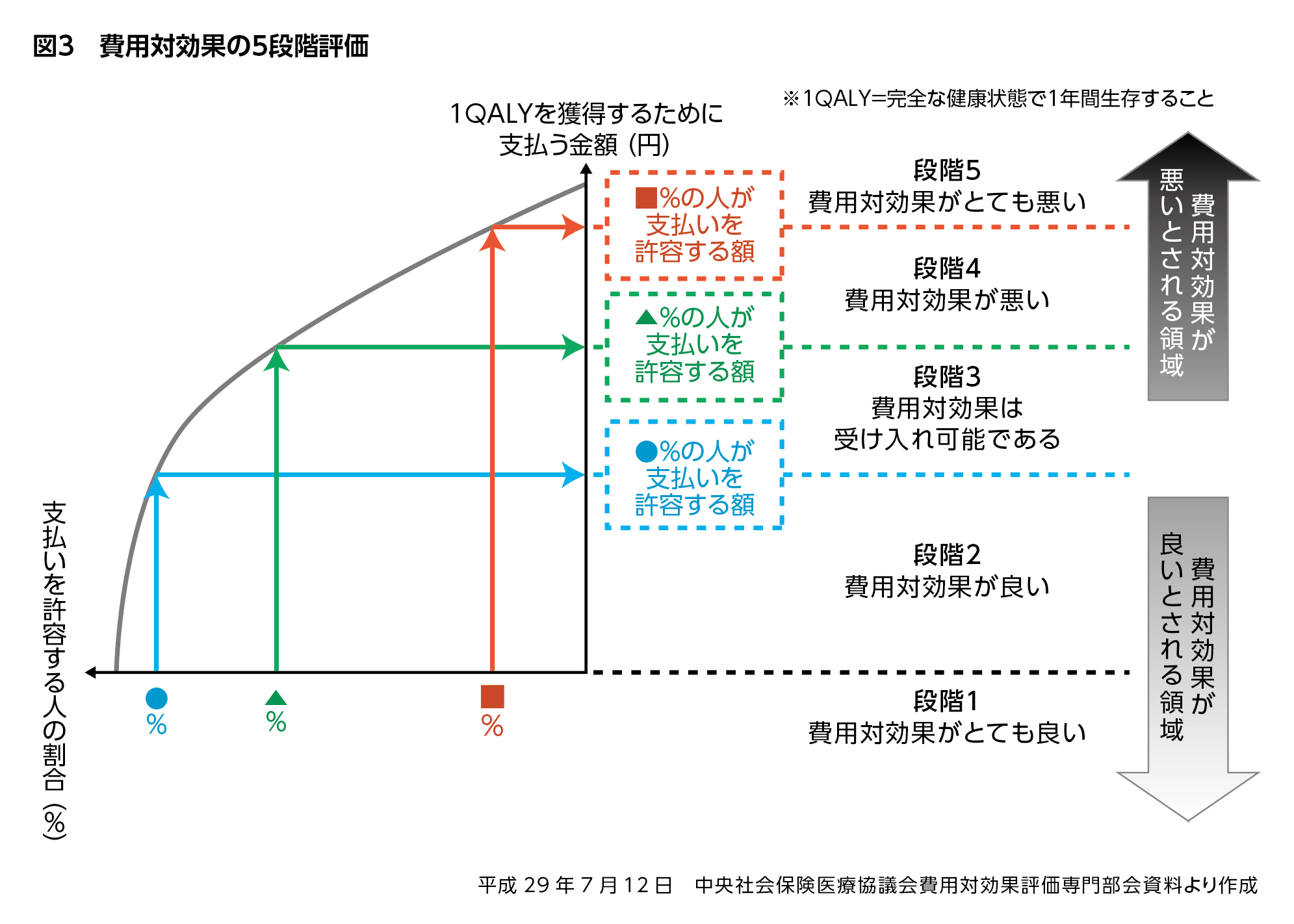
費用対効果評価は最終的に、「費用対効果がとても良い」から「費用対効果がとても悪い」まで5段階で示される予定ですが(図3)、評価の際に必要となる基準の値を設定する方法として、患者の支払い意思額を基本とし、国民一人当たりのGDPなども目安に考える提案がなされています。
しかし、この金額は患者の経済状態や健康に対する考え方によって大きく異なり、一律な金額を決めることは困難です。
そこで専門部会では、支払い意思額についてのアンケート調査を参考にする案が出ています。
「支払い意思額」あなたはどう答える?
ある人が病気にかかっており、死が迫っています。しかし、この病気に対する新しい治療法が開発されました。この治療を受ければ、完全に健康な状態で1年間だけ寿命を延ばすことができます。この治療法の費用を公的医療保険から支払おうと考えています。
アンケート調査では、医療機関の窓口で支払う料金ではなく、公的医療保険として支払う医療費についての質問とし、公的医療保険から支払われる治療費の費用に応じてあなたが負担する保険料は増加する可能性があるという前提で、上記の状況設定がされています。
この治療費をx円とし、公的医療保険から支出すべきか、そしてx円より高い金額(y円)と低い金額(z円)になった場合ではどうかと質問が続きます。
あなたが回答者になったとしたら、この質問に戸惑うのではないでしょうか。治療に対する金銭感覚や1年間の延命に対する価値観もさまざまでしょうし、捉えようによっては命の金額を問うているようにも思えます。治療の対象者は他人と想定して回答してもらう方向ですが、調査の内容については専門部会内でも異論が噴出しています。
11月以降の制度化の議論とあわせ、実施のあり方や調査内容については引き続き検討されることになります。
高額薬剤のアクセス制限
活高額薬剤の薬価特例引き下げ
保険医療財政を脅かすのではないかと指摘される高額薬剤も近年のトピックスです。
2016年4月の薬価改定では、C型慢性肝炎の画期的新薬として登場したソバルディとハーボニーが特例再算定の対象に指定され、31.7%の大幅薬価引き下げとなりました。
最新の抗がん剤として脚光を浴びている免疫チェックポイント阻害薬(オプジーボ、キイトルーダ)は、高薬価が設定され、発売初年度の売上実績が当初の売り上げ見込みを大幅に上回ったことから、次期改定2018年4月を待たずに異例のスピードで薬価が引き下げられ、引き下げ幅も算定ルール最大の50%とされました(2017年2月1日より適用)。
薬価引き下げによる影響は製薬企業にとって経営を左右する大きな問題です。持続可能な医療提供を堅持するために医療費の拡大を引き締めることは避けて通れませんが、製薬企業の経営や開発への影響が大きくなればなるほど、患者さんに必要な医薬品を届けるという使命を果たせなくなるリスクも大きくなります。
高額であるために患者さんの使用機会を喪失することもアクセス制限ですが、必要な薬の開発が阻害され患者さんの利益を損なうことも、アクセス制限といえるでしょう。
「最適使用推進ガイドライン」
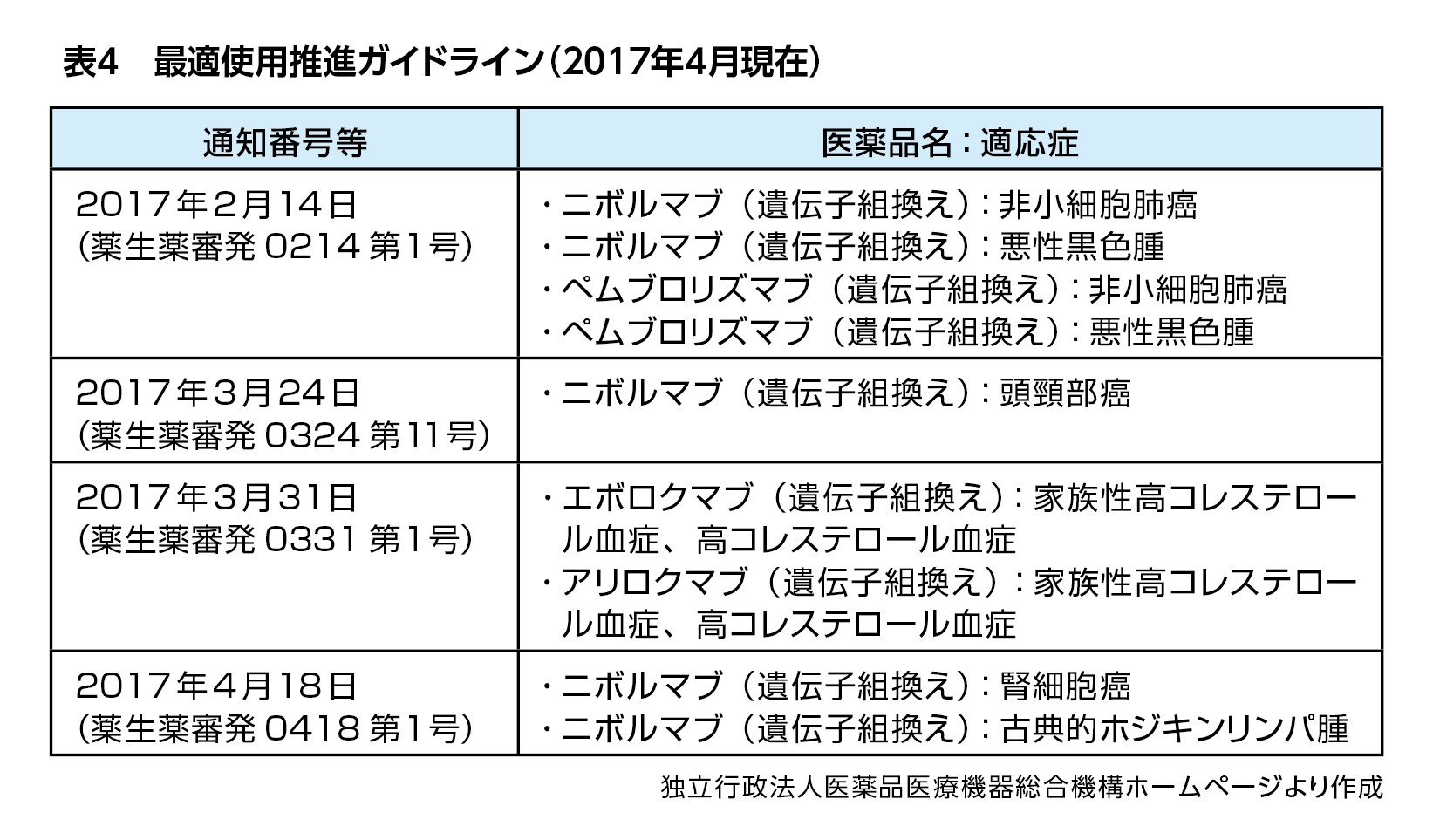
「経済財政運営と改革の基本方針2016」に革新的医薬品の使用の最適化推進を図ることが盛り込まれたことを受け、革新的医薬品を真に必要な患者に提供するために「最適使用推進ガイドライン」(表4)が策定されることになりました。これには、高額薬剤の使用患者や扱う医師・施設を絞る意図があります。
最適使用推進ガイドラインには、その医薬品の使用が最適と考えられる患者の選択基準と、その医薬品を適切に使用できる医師・医療機関等の要件が規定されています。また、作成に伴い当該医薬品の保険適用上の留意事項が示され、ガイドライン作成済み医薬品の適正使用に向けて、より厳格な運用が求められます。
国民皆保険制度と医薬品アクセス
医薬品アクセスへの国民の権利
日本の国民皆保険制度の特徴は、国民全員を公的医療保険で保障する、医療機関を自由に選べる(フリーアクセス)、安い医療費で高度な医療が受けられる、社会保険方式を基本としつつ皆保険を維持するため公費を投入している、などが挙げられます。
1960年代からほぼ半世紀、この国民皆保険制度のもと、誰もが安心して医療を受けられる医療制度を実現し、世界最高レベルの平均寿命と保健医療水準を達成してきた日本では、少子高齢化、経済情勢の変化に対応し、引き続き持続可能な公的医療保険制度の維持を模索しています。
医薬品へのアクセスについても、こうした国民の権利が保証される制度でなければなりません。
イノベーションと医薬品アクセスのバランス
がんやアルツハイマーなど、生命を脅かしQOLを著しく損なう恐れのある疾患では、治療効果を飛躍的に高める画期的な新薬の登場が期待されています。
国は医薬品産業を、経済成長を担う重要な産業であると位置づけて強化戦略を立てる一方で、限りある医療財源をいかに効率化するかという難しい問題に直面しています。医療費抑制のため、イノベーションの適切な評価推進の流れは今後も続くでしょう。患者さんの利益の最大化のため、イノベーションと医薬品アクセスのバランスをいかに取るかが、国や製薬企業の新たな課題といえるかもしれません。
MRが情報提供する際には、有効性・安全性に加え、より費用対効果を意識した医薬品情報を提供する必要が出てくるでしょう。
参考資料
- 医薬産業政策研究所リサーチペーパー・シリーズNo.40「日本におけるドラッグ・ラグに関する調査」(2008年6月)
- 第220回中央社会保険医療協議会総会資料「答申書(平成24年度診療報酬改定について)」(2012年2月10日)
- 第37回中央社会保険医療協議会費用対効果評価専門部会資料「既収載品にかかる対象品目の選定基準と対象品目」(2017年2月8日)
- 第40回中央社会保険医療協議会費用対効果評価専門部会資料「医薬品の費用対効果評価の一定の仮定をおいたイメージ」(2017年6月14日)
- 第39回中央社会保険医療協議会費用対効果評価専門部会資料「総合的評価(アプレイザル)について」(2017年5月31日)
- 第43回中央社会保険医療協議会費用対効果評価専門部会資料「費用対効果評価の制度化に向けたこれまでの議論のまとめ(案)」・「費用対効果評価の制度化に向けた検討(その7)<支払い意思額について>」・「「国内の支払い意思額に関する調査」調査票(案)」(2017年7月12日)
- 独立行政法人医薬品医療機器総合機構ホームページ